Какое пламя горячее синее или красное
Какое пламя горячее синее или красное

Всегда кажется, что огонь имеет два оттенка – красный и желтый. Но если присмотреться внимательно, то можно приметить, что цветность огня различается от того, какой предмет горит. Входящие в его состав вещества и выдают свои цвета пламени. Итак, почему огонь бывает разного цвета, от чего зависит цвет пламени?

Что такое пламя и почему огонь бывает разного цвета
Языки пламени представлены в виде раскаленных газов, иногда содержащих плазму и твердые элементы, в которых совершаются физико-химические перевоплощения реагентных элементов, вызывающие свечение, выделение тепла, самостоятельный нагрев.
Газообразная среда пламени состоит из заряженных ионов и радикалов, что объясняет возможность электропроводности пламени и его взаимодействие с электромагнитными полями. По такому принципу производятся приборы, обладающие способностью при помощи электромагнитного излучения приглушать пламя, оторвать его от горючих материалов и даже изменить форму.
Причины разноцветности пламени
Почему включив газовую конфорку и поджигая выходящий газ, мы видим голубоватый огонь? В процессе горения газ распадается на кислород и углерод, выделяя при этом угарный газ, который и является причиной голубого цвета.

Почему подожженная простая пищевая соль – в огне выдает желтые и красные цвета? В состав соли входит хлорид натрия, при горении создающий желто-оранжевые языки пламени. Любой деревянный предмет или костер из дров будут гореть таким же цветом, так как в составе древесного материала находится большое количество подобных солей.

Есть у огня и зеленые оттенки, почему? Их появление означает то, что в горящих предметах содержатся фосфор или медь. Причем медное пламя будет ярким и слепящим, близким к белому. Причиной зеленого пламени может стать наличие в предметах горения бария, молибдена, фосфора, сурьмы. Синий цвет зависит от селена или бора.

Огонь без признаков цвета можно увидеть только в лабораторных условиях. Понять, что что-то горит, возможно только по легкому колебанию воздуха и выделяемому теплу.
Полезно знать
- Все газовые приборы представляют собой повышенную опасность. По этой причине не помешает узнать некоторые признаки поломок, способы их устранения. Определять неисправности будем по цвету пламени.
- Если ваша горелка при работе издает желтое пламя или оранжевое – это признак того, что не хватает воздушной смеси. Чтобы горение газа проходило правильно, максимально выдавала тепло, необходимо достаточное количество воздуха, который перемешивается с газом в главной горелке.
- Нарушение баланса в смеси топлива и воздуха может произойти по разным причинам. Воздушные отверстия засорились пылью, не давая проходить воздушным потокам. Пылевые накопления, сгорая, создают желтоватый или оранжевый цвет пламени.
- Желтизна пламени возможна и в том случае, газовое оборудование приобретено неправильно. При сгорании любого топлива выделяется угарный газ. Колонки, выдающие при работе синее пламя, выдают низкий уровень СО. Наличие оранжевого или красного огня говорят об обратном.
- При отравлении угарными газами наблюдаются симптомы, как при гриппе – головные боли, тошнота, головокружения. Угарный газ опасен тем, что его присутствие зачастую остается незамеченным людьми, так как он не отличается наличием цвета или запаха.

Теперь вы знаете, почему огонь бывает разного цвета, от чего зависит цвет пламени. Обратите внимание: если мы наблюдаем на газовом приборе желтое, красное или оранжевое пламя – это можно считать сигналом опасности. Обнаружив это, необходимо вызвать квалифицированных специалистов, которые определят причину и устранят неисправность газового оборудования.
Пламя бывает разного цвета. Посмотрите в камин. На поленьях пляшут желтые, оранжевые, красные, белые и синие языки пламени. Его цвет зависит от температуры горения и от горючего материала. Чтобы наглядно себе это представить, вообразите спираль электрической плитки. Если плитка выключена — витки спирали холодные и черные. Допустим, вы решили подогреть суп и включили плитку. Сначала спираль становится темно-красной. Чем выше поднимается температура, тем ярче красный цвет спирали. Когда плитка разогревается до максимальной температуры, спираль становится оранжево-красной.
Естественно, спираль не горит. Вы же не видите пламени. Она просто очень горячая. Если нагревать ее дальше, то будет меняться и цвет. Сначала цвет спирали станет желтым, затем белым, а когда она раскалится еще больше, от нее будет исходить голубое сияние.
От чего зависит цвет пламени
Нечто подобное происходит и с пламенем. Возьмем для примера свечу. Различные участки пламени свечи имеют разную температуру. Огню нужен кислород. Если свечу накрыть стеклянной банкой, огонь погаснет. Центральный, прилегающий к фитилю участок пламени свечи, потребляет мало кислорода, и выглядит темным. Верхушке и боковым участкам пламени достается больше кислорода, поэтому эти участки ярче.
По мере того как пламя продвигается по фитилю, воск тает и потрескивает, рассыпаясь на мельчайшие частички углерода. (Каменный уголь тоже состоит из углерода.) Эти частички увлекаются пламенем кверху и сгорают. Они очень горячие и светятся, как спираль вашей плитки. Но частички углерода намного горячее, чем спираль самой жаркой плитки (температура сгорания углерода примерно 1 400 градусов Цельсия). Поэтому свечение их имеет желтый цвет. Около горящего фитиля пламя еще горячее и светится синим цветом.
Пламя камина или костра в основном пестрого вида. Дерево горит при более низкой температуре, чем фитиль свечи, поэтому основной цвет костра — оранжевый, а не желтый. Некоторые частички углерода в пламени костра имеют довольно высокую температуру. Их немного, но они добавляют пламени желтоватый оттенок. Остывшие частички раскаленного углерода — это копоть, которая оседает на печных трубах. Температура горения дерева ниже температуры горения свечи. Кальций, натрий и медь, нагретые до высокой температуры, светятся разными цветами. Их добавляют в порох ракет для расцвечивания огней праздничных фейерверков.
Цвет пламени и химический состав
Цвет пламени может меняться в зависимости от химических примесей, содержащихся в поленьях или другом горючем веществе. В пламени может находиться, например, примесь натрия. Натрий — это составная часть поваренной соли. Если натрий раскалить, он окрашивается в ярко – желтый цвет. В огонь может попасть кальций.
Мы все знаем, что кальция много в молоке. Это металл. Раскаленный кальций окрашивается в яркий красный цвет. Если в огне горит фосфор, то пламя окрасится в зеленоватый цвет. Все эти элементы или содержатся в дереве, или попадают в огонь с другими веществами. Смешение цветов пламени, как и смешение цветов радуги, может дать белый цвет, поэтому в пламени костра или камина видны белые участки.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.

Пламя бывает разного цвета. Посмотрите в камин. На поленьях пляшут желтые, оранжевые, красные, белые и синие языки пламени. Его цвет зависит от температуры горения и от горючего материала. Чтобы наглядно себе это представить, вообразите спираль электрической плитки. Если плитка выключена — витки спирали холодные и черные. Допустим, вы решили подогреть суп и включили плитку. Сначала спираль становится темно-красной. Чем выше поднимается температура, тем ярче красный цвет спирали. Когда плитка разогревается до максимальной температуры, спираль становится оранжево-красной.
Естественно, спираль не горит. Вы же не видите пламени. Она просто очень горячая. Если нагревать ее дальше, то будет меняться и цвет. Сначала цвет спирали станет желтым, затем белым, а когда она раскалится еще больше, от нее будет исходить голубое сияние.

Нечто подобное происходит и с пламенем. Возьмем для примера свечу. Различные участки пламени свечи имеют разную температуру. Огню нужен кислород. Если свечу накрыть стеклянной банкой, огонь погаснет. Центральный, прилегающий к фитилю участок пламени свечи, потребляет мало кислорода, и выглядит темным. Верхушке и боковым участкам пламени достается больше кислорода, поэтому эти участки ярче. По мере того как пламя продвигается по фитилю, воск тает и потрескивает, рассыпаясь на мельчайшие частички углерода. (Каменный уголь тоже состоит из углерода.) Эти частички увлекаются пламенем кверху и сгорают. Они очень горячие и светятся, как спираль вашей плитки. Но частички углерода намного горячее, чем спираль самой жаркой плитки (температура сгорания углерода примерно 1 400 градусов Цельсия). Поэтому свечение их имеет желтый цвет. Около горящего фитиля пламя еще горячее и светится синим цветом.
Пламя камина или костра в основном пестрого вида. Дерево горит при более низкой температуре, чем фитиль свечи, поэтому основной цвет костра — оранжевый, а не желтый. Некоторые частички углерода в пламени костра имеют довольно высокую температуру. Их немного, но они добавляют пламени желтоватый оттенок. Остывшие частички раскаленного углерода — это копоть, которая оседает на печных трубах. Температура горения дерева ниже температуры горения свечи. Кальций, натрий и медь, нагретые до высокой температуры, светятся разными цветами. Их добавляют в порох ракет для расцвечивания огней праздничных фейерверков.
Цвет пламени и химический состав
Цвет пламени может меняться в зависимости от химических примесей, содержащихся в поленьях или другом горючем веществе. В пламени может находиться, например, примесь натрия.

Еще в древние времена ученые и алхимики пытались понять, что за вещества сгорают в огне, в зависимости от того, в какой цвет окрашивался огонь.
- Натрий — это составная часть поваренной соли. Если натрий раскалить, он окрашивается в ярко — желтый цвет.
- В огонь может попасть кальций. Мы все знаем, что кальция много в молоке. Это металл. Раскаленный кальций окрашивается в яркий красный цвет.
- Если в огне горит фосфор, то пламя окрасится в зеленоватый цвет. Все эти элементы или содержатся в дереве, или попадают в огонь с другими веществами.
- Практически у всех дома есть газовые плиты или колонки, пламя в которых окрашено в голубой оттенок. Это обусловлено сгораемым углеродом, угарным газом, который и дает этот оттенок.

Смешение цветов пламени, как и смешение цветов радуги, может дать белый цвет, поэтому в пламени костра или камина видны белые участки.
Температура пламени при горении некоторых веществ:
Химия пламени
Чем проклинать тьму,
лучше зажечь хотя бы
одну маленькую свечу.
Конфуций

В начале
Первые попытки понять механизм горения связаны с именами англичанина Роберта Бойля, француза Антуана Лорана Лавуазье и русского Михаила Васильевича Ломоносова. Оказалось, что при горении вещество никуда не «исчезает», как наивно полагали когда-то, а превращается в другие вещества, в основном газообразные и потому невидимые. Лавуазье в 1774 году впервые показал, что при горении из воздуха уходит примерно пятая его часть. В течение XIX века ученые подробно исследовали физические и химические процессы, сопровождающие горение. Необходимость таких работ была вызвана прежде всего пожарами и взрывами в шахтах.
Но только в последней четверти ХХ века были выявлены основные химические реакции, сопровождающие горение, и по сей день в химии пламени осталось немало темных пятен. Их исследуют самыми современными методами во многих лабораториях. У этих исследований несколько целей. С одной стороны, надо оптимизировать процессы горения в топках ТЭЦ и в цилиндрах двигателей внутреннего сгорания, предотвратить взрывное горение (детонацию) при сжатии в цилиндре автомобиля воздушно-бензиновой смеси. С другой стороны, необходимо уменьшить количество вредных веществ, образующихся в процессе горения, и одновременно — искать более эффективные средства тушения огня.
Существуют два вида пламени. Топливо и окислитель (чаще всего кислород) могут принудительно или самопроизвольно подводиться к зоне горения порознь и смешиваться уже в пламени. А могут смешиваться заранее — такие смеси способны гореть или даже взрываться в отсутствие воздуха, как, например, пороха, пиротехнические смеси для фейерверков, ракетные топлива. Горение может происходить как с участием кислорода, поступающего в зону горения с воздухом, так и при помощи кислорода, заключенного в веществе-окислителе. Одно из таких веществ — бертолетова соль (хлорат калия KClO3); это вещество легко отдает кислород. Сильный окислитель — азотная кислота HNO3: в чистом виде она воспламеняет многие органические вещества. Нитраты, соли азотной кислоты (например, в виде удобрения — калийной или аммиачной селитры), легко воспламеняются, если смешаны с горючими веществами. Еще один мощный окислитель, тетраоксид азота N2O4 — компонент ракетных топлив. Кислород могут заменить и такие сильные окислители, как, например, хлор, в котором горят многие вещества, или фтор. Чистый фтор — один из самых сильных окислителей, в его струе горит вода.
Цепные реакции
Основы теории горения и распространения пламени были заложены в конце 20-х годов прошлого столетия. В результате этих исследований были открыты разветвленные цепные реакции. За это открытие отечественный физикохимик Николай Николаевич Семенов и английский исследователь Сирил Хиншельвуд были в 1956 году удостоены Нобелевской премии по химии. Более простые неразветвленные цепные реакции открыл еще в 1913 году немецкий химик Макс Боденштейн на примере реакции водорода с хлором. Суммарно реакция выражается простым уравнением H2 + Cl2 = 2HCl. На самом деле она идет с участием очень активных осколков молекул — так называемых свободных радикалов. Под действием света в ультрафиолетовой и синей областях спектра или при высокой температуре молекулы хлора распадаются на атомы, которые и начинают длинную (иногда до миллиона звеньев) цепочку превращений; каждое из этих превращений называется элементарной реакцией:
Cl + H2 → HCl + H,
H + Cl2 → HCl + Cl и т. д.
На каждой стадии (звене реакции) происходит исчезновение одного активного центра (атома водорода или хлора) и одновременно появляется новый активный центр, продолжающий цепь. Цепи обрываются, когда встречаются две активные частицы, например Cl + Cl → Cl2. Каждая цепь распространяется очень быстро, поэтому, если генерировать «первоначальные» активные частицы с высокой скоростью, реакция пойдет так быстро, что может привести к взрыву.
Н. Н. Семенов и Хиншельвуд обнаружили, что реакции горения паров фосфора и водорода идут иначе: малейшая искра или открытое пламя могут вызвать взрыв даже при комнатной температуре. Эти реакции — разветвленно-цепные: активные частицы в ходе реакции «размножаются», то есть при исчезновении одной активной частицы появляются две или три. Например, в смеси водорода и кислорода, которая может спокойно храниться сотни лет, если нет внешних воздействий, появление по той или иной причине активных атомов водорода запускает такой процесс:
Таким образом, за ничтожный промежуток времени одна активная частица (атом H) превращается в три (атом водорода и два гидроксильных радикала OH), которые запускают уже три цепи вместо одной. В результате число цепей лавинообразно растет, что моментально приводит к взрыву смеси водорода и кислорода, поскольку в этой реакции выделяется много тепловой энергии. Атомы кислорода присутствуют в пламени и при горении других веществ. Их можно обнаружить, если направить струю сжатого воздуха поперек верхней части пламени горелки. При этом в воздухе обнаружится характерный запах озона — это атомы кислорода «прилипли» к молекулам кислорода с образованием молекул озона: О + О2 = О3, которые и были вынесены из пламени холодным воздухом.

Возможность взрыва смеси кислорода (или воздуха) со многими горючими газами — водородом, угарным газом, метаном, ацетиленом — зависит от условий, в основном от температуры, состава и давления смеси. Так, если в результате утечки бытового газа на кухне (он состоит в основном из метана) его содержание в воздухе превысит 5%, то смесь взорвется от пламени спички или зажигалки и даже от маленькой искры, проскочившей в выключателе при зажигании света. Взрыва не будет, если цепи обрываются быстрее, чем успевают разветвляться. Именно поэтому была безопасной лампа для шахтеров, которую английский химик Хэмфри Дэви разработал в 1816 году, ничего не зная о химии пламени. В этой лампе открытый огонь был отгорожен от внешней атмосферы (которая могла оказаться взрывоопасной) частой металлической сеткой. На поверхности металла активные частицы эффективно исчезают, превращаясь в стабильные молекулы, и потому не могут проникнуть во внешнюю среду.
Полный механизм разветвленно-цепных реакций очень сложен и может включать более сотни элементарных реакций. К разветвленно-цепным относятся многие реакции окисления и горения неорганических и органических соединений. Таковой же будет и реакция деления ядер тяжелых элементов, например плутония или урана, под воздействием нейтронов, которые выступают аналогами активных частиц в химических реакциях. Проникая в ядро тяжелого элемента, нейтроны вызывают его деление, что сопровождается выделением очень большой энергии; одновременно из ядра вылетают новые нейтроны, которые вызывают деление соседних ядер. Химические и ядерные разветвленно-цепные процессы описываются сходными математическими моделями.
Что надо для начала
Чтобы началось горение, нужно выполнить ряд условий. Прежде всего, температура горючего вещества должна превышать некое предельное значение, которое называется температурой воспламенения. Знаменитый роман Рэя Брэдбери «451 градус по Фаренгейту» назван так потому, что примерно при этой температуре (233°C) загорается бумага. Это «температура воспламенения», выше которой твердое топливо выделяет горючие пары или газообразные продукты разложения в количестве, достаточном для их устойчивого горения. Примерно такая же температура воспламенения и у сухой сосновой древесины.

Температура пламени зависит от природы горючего вещества и от условий горения. Так, температура в пламени метана на воздухе достигает 1900°C, а при горении в кислороде — 2700°C. Еще более горячее пламя дают при сгорании в чистом кислороде водород (2800°C) и ацетилен (3000°C). Недаром пламя ацетиленовой горелки легко режет почти любой металл. Самую же высокую температуру, около 5000°C (она зафиксирована в Книге рекордов Гиннесса), дает при сгорании в кислороде легкокипящая жидкость — субнитрид углерода С4N2 (это вещество имеет строение дицианоацетилена NC–C=C–CN). А по некоторым сведениям, при горении его в атмосфере озона температура может доходить до 5700°C. Если же эту жидкость поджечь на воздухе, она сгорит красным коптящим пламенем с зелено-фиолетовой каймой. С другой стороны, известны и холодные пламена. Так, например, горят при низких давлениях пары фосфора. Сравнительно холодное пламя получается и при окислении в определенных условиях сероуглерода и легких углеводородов; например, пропан дает холодное пламя при пониженном давлении и температуре от 260–320°C.
Только в последней четверти ХХ века стал проясняться механизм процессов, происходящих в пламени многих горючих веществ. Механизм этот очень сложен. Исходные молекулы обычно слишком велики, чтобы, реагируя с кислородом, непосредственно превратиться в продукты реакции. Так, например, горение октана, одного из компонентов бензина, выражается уравнением 2С8Н18 + 25О2 = 16СО2 + 18Н2О. Однако все 8 атомов углерода и 18 атомов водорода в молекуле октана никак не могут одновременно соединиться с 50 атомами кислорода: для этого должно разорваться множество химических связей и образоваться множество новых. Реакция горения происходит многостадийно — так, чтобы на каждой стадии разрывалось и образовывалось лишь небольшое число химических связей, и процесс состоит из множества последовательно протекающих элементарных реакций, совокупность которых и представляется наблюдателю как пламя. Изучать элементарные реакции сложно прежде всего потому, что концентрации реакционно-способных промежуточных частиц в пламени крайне малы.
Внутри пламени
Оптическое зондирование разных участков пламени с помощью лазеров позволило установить качественный и количественный состав присутствующих там активных частиц — осколков молекул горючего вещества. Оказалось, что даже в простой с виду реакции горения водорода в кислороде 2Н2 + О2 = 2Н2О происходит более 20 элементарных реакций с участием молекул О2, Н2, О3, Н2О2, Н2О, активных частиц Н, О, ОН, НО2. Вот, например, что написал об этой реакции английский химик Кеннет Бэйли в 1937 году: «Уравнение реакции соединения водорода с кислородом — первое уравнение, с которым знакомится большинство начинающих изучать химию. Реакция эта кажется им очень простой. Но даже профессиональные химики бывают несколько поражены, увидев книгу в сотню страниц под названием «Реакция кислорода с водородом», опубликованную Хиншельвудом и Уильямсоном в 1934 году». К этому можно добавить, что в 1948 году была опубликована значительно большая по объему монография А. Б. Налбандяна и В. В. Воеводского под названием «Механизм окисления и горения водорода».
Современные методы исследования позволили изучить отдельные стадии подобных процессов, измерить скорость, с которой различные активные частицы реагируют друг с другом и со стабильными молекулами при разных температурах. Зная механизм отдельных стадий процесса, можно «собрать» и весь процесс, то есть смоделировать пламя. Сложность такого моделирования заключается не только в изучении всего комплекса элементарных химических реакций, но и в необходимости учитывать процессы диффузии частиц, теплопереноса и конвекционных потоков в пламени (именно последние устраивают завораживающую игру языков горящего костра).
Откуда все берется
Основное топливо современной промышленности — углеводороды, начиная от простейшего, метана, и кончая тяжелыми углеводородами, которые содержатся в мазуте. Пламя даже простейшего углеводорода — метана может включать до ста элементарных реакций. При этом далеко не все из них изучены достаточно подробно. Когда горят тяжелые углеводороды, например те, что содержатся в парафине, их молекулы не могут достичь зоны горения, оставаясь целыми. Еще на подходе к пламени они из-за высокой температуры расщепляются на осколки. При этом от молекул обычно отщепляются группы, содержащие два атома углерода, например С8Н18 → С2Н5 + С6Н13. Активные частицы с нечетным числом атомов углерода могут отщеплять атомы водорода, образуя соединения с двойными С=С и тройными С≡С связями. Было обнаружено, что в пламени такие соединения могут вступать в реакции, которые не были ранее известны химикам, поскольку вне пламени они не идут, например С2Н2 + О → СН2 + СО, СН2 + О2 → СО2 + Н + Н.
Постепенная потеря водорода исходными молекулами приводит к увеличению в них доли углерода, пока не образуются частицы С2Н2, С2Н, С2. Зона сине-голубого пламени обусловлена свечением в этой зоне возбужденных частиц С2 и СН. Если доступ кислорода в зону горения ограничен, то эти частицы не окисляются, а собираются в агрегаты — полимеризуются по схеме С2Н + С2Н2 → С4Н2 + Н, С2Н + С4Н2 → С6Н2 + Н и т. д.
В результате образуются частицы сажи, состоящие почти исключительно из атомов углерода. Они имеют форму крошечных шариков диаметром до 0,1 микрометра, которые содержат примерно миллион атомов углерода. Такие частицы при высокой температуре дают хорошо светящееся пламя желтого цвета. В верхней части пламени свечи эти частицы сгорают, поэтому свеча не дымит. Если же происходит дальнейшее слипание этих аэрозольных частиц, то образуются более крупные частицы сажи. В результате пламя (например, горящей резины) дает черный дым. Такой дым появляется, если в исходном топливе повышена доля углерода относительно водорода. Примером могут служить скипидар — смесь углеводородов состава С10Н16 (CnH2n–4), бензол С6Н6 (CnH2n–6), другие горючие жидкости с недостатком водорода — все они при горении коптят. Коптящее и ярко светящее пламя дает горящий на воздухе ацетилен С2Н2 (CnH2n–2); когда-то такое пламя использовали в ацетиленовых фонарях, установленных на велосипедах и автомобилях, в шахтерских лампах. И наоборот: углеводороды с высоким содержанием водорода — метан СН4, этан С2Н6, пропан С3Н8, бутан С4Н10 (общая формула CnH2n+2) — горят при достаточном доступе воздуха почти бесцветным пламенем. Смесь пропана и бутана в виде жидкости под небольшим давлением находится в зажигалках, а также в баллонах, которые используют дачники и туристы; такие же баллоны установлены в автомобилях, работающих на газе. Сравнительно недавно было обнаружено, что в копоти часто присутствуют шарообразные молекулы, состоящие из 60 атомов углерода; их назвали фуллеренами, а открытие этой новой формы углерода было ознаменовано присуждением в 1996 году Нобелевской премии по химии.
Пламя
Пламя – это газообразная среда, в которой происходит взаимодействие горючего и окислителя, выделяется тепло и развиваются высокие температуры.
Классификация
Пламя классифицируют по:
- агрегатному состоянию горючих веществ: пламя газообразных, жидких, твердых и аэродисперсных реагентов;
- излучению: светящиеся, окрашенные, бесцветные;
- состоянию среды горючее-окислитель: диффузионные, предварительно перемешанных сред;
- характеру перемещения реакционной среды: ламинарные, турбулентные, пульсирующие;
- температуре: холодные, низкотемпературные, высокотемпературные;
- скорости распространения: медленные, быстрые;
- высоте: короткие, длинные;
- визуальному восприятию: коптящие, прозрачные, цветные.
В ламинарном диффузионном пламени можно выделить 3 зоны (оболочки).
Внутри конуса пламени имеются:
- темная зона (300-350 °С), где горение не происходит из-за недостатка окислителя;
- светящаяся зона, где происходит термическое разложение горючего и частичное его сгорание (500-800 °С);
- едва светящаяся зона, которая характеризуется окончательным сгоранием продуктов разложения горючего и максимальной температурой (900-1500 °С).
Температура
Температура пламени зависит от природы горючего вещества и интенсивности подвода окислителя. Например:
- Температура воспламенения для большинства твёрдых материалов – 300 °С.
- Температура пламени в горящей сигарете – 250-300 °С.
- Температура пламени спички 750-1400 °С; при этом 300 °С – температура воспламенения дерева, а температура горения дерева равняется примерно 800–1000 °С.
- Температура горения пропан-бутана – 800-1970 °С.
- Температура пламени керосина – 800 °С, в среде чистого кислорода – 2000 °С.
- Температура горения бензина – 1300-1400 °С.
- Температура пламени спирта не превышает 900 °С.
- Температура горения магния – 2200 °С; значительная часть излучения в УФ-диапазоне.
Наиболее высокие известные температуры горения:
- дицианоацетилен C4N2 5260 К (4990 °C) в кислороде и до 6000 К (5730 °C) в озоне;
- дициан (CN)2 4525 °C в кислороде.
Так как вода обладает очень большой теплоёмкостью, отсутствие водорода в горючем исключает потери тепла на образование воды и позволяет развить большую температуру.
Скорость распространения
Распространение пламени по предварительно перемешанной среде (невозмущенной), происходит от каждой точки фронта пламени по нормали к поверхности пламени. Величина такой нормальной скорости распространения пламени (далее – НСРП) является основной характеристикой горючей среды. Она представляет собой минимальную возможную скорость пламени. Значения НСРП отличаются у различных горючих смесей – от 0,03 до 15 м/с.
Распространение пламени по реально существующим газовоздушным смесям всегда осложнено внешними возмущающими воздействиями, обусловленными силами тяжести, конвективными потоками, трением и т.д. Поэтому реальные скорости распространения пламени всегда отличаются от нормальных. В зависимости от характера горения скорости распространения пламени имеют следующие диапазоны величин при:
- дефлаграционном горении – до 100 м/с;
- взрывном горении – от 300 до 1000 м/с;
- детонационном горении – свыше 1000 м/с.
Цвет пламени определяется излучением электронных переходов (например, тепловым излучением) различных возбужденных (как заряженных, так и незаряженных) частиц, образующихся в результате химической реакции между молекулами горючего и кислородом воздуха, а также в результате термической диссоциации. В частности, при горении углеродного горючего в воздухе, синяя часть цвета пламени обусловлена излучением частиц CN ±n , красно-оранжевая — излучением частиц С2 ±n и микрочастиц сажи. Излучение прочих образующихся в процессе горения частиц (CHx ±n , H2O ±n , HO ±n , CO2 ±n , CO ±n ) и основных газов (N2, O2, Ar) лежит в невидимой для человеческого глаза УФ и ИК части спектра. Кроме того, на окраску пламени сильно влияет присутствие в самом топливе, деталях конструкции горелок, сопел и так далее соединений различных металлов, в первую очередь натрия. В видимой части спектра излучение натрия крайне интенсивно и ответственно за оранжево-желтый цвет пламени, при этом излучение чуть менее распространенного калия оказывается на его фоне практически не различимым (поскольку большинство организмов имеют в составе клеток K+/Na+ каналы, то в углеродном горючем растительного или животного происхождения на 3 атома натрия приходится в среднем 2 атома калия).
Источник: Тидеман Б.Е., Сциборский Д.Б. Химия горения. –Л., 1935.
Пламя: строение, описание, схема, температура
В процессе горения образуется пламя, строение которого обусловлено реагирующими веществами. Его структура поделена на области в зависимости от температурных показателей.
Определение
Пламенем называют газы в раскаленном виде, в которых присутствуют составляющие плазмы или вещества в твердой дисперсной форме. В них осуществляются преобразования физического и химического типа, сопровождающиеся свечением, выделением тепловой энергии и разогревом.
Наличие же в газообразной среде ионных и радикальных частичек характеризует его электрическую проводимость и особое поведение в электромагнитном поле.

Что такое языки пламени
Обычно так называют процессы, связанные с горением. По сравнению с воздухом, газовая плотность меньше, но высокие температурные показатели обуславливают поднятие газа. Так и образуются языки пламени, которые бывают длинными и короткими. Часто происходит и плавный переход одних форм в другие.
Пламя: строение и структура
Для определения внешнего вида описываемого явления достаточно зажечь газовую горелку. Появившееся несветящееся пламя нельзя назвать однородным. Визуально можно выделить три его основные области. Кстати, изучение строения пламени показывает, что различные вещества горят с образованием различного типа факела.
При горении смеси из газа и воздуха вначале происходит формирование короткого факела, цвет которого имеет голубые и фиолетовые оттенки. В нем просматривается ядро — зелено-голубое, напоминающее конус. Рассмотрим это пламя. Строение его разделяется на три зоны:
- Выделяют подготовительную область, в которой происходит нагревание смеси из газа и воздуха при выходе из отверстия горелки.
- За ней следует зона, в которой происходит горение. Она занимает верхушку конуса.
- Когда имеется недостаток воздушного потока, газ сгорает не полностью. Выделяется углерода двухвалентный оксид и водородные остатки. Их догорание протекает в третьей области, где есть кислородный доступ.
Теперь отдельно рассмотрим разные процессы горения.
Горение свечи
Горение свечи подобно горению спички или зажигалки. А строение пламени свечи напоминает раскаленный газовый поток, который вытягивается вверх за счет выталкивающих сил. Процесс начинается с нагревания фитиля, за которым следует испарение парафина.
Самую нижнюю зону, находящуюся внутри и прилегающую к нити, называют первой областью. Она обладает небольшим свечением синего цвета из-за большого количества топлива, но малого объема кислородной смеси. Здесь осуществляется процесс неполного сгорания веществ с выделением угарного газа, который в дальнейшем окисляется.

Первую зону окружает светящаяся вторая оболочка, характеризующая строение пламени свечи. В нее поступает больший кислородный объем, что обуславливает продолжение окислительной реакции с участием топливных молекул. Температурные показатели здесь будут выше, чем в темной зоне, но недостаточные для конечного разложения. Именно в первых двух областях при сильном нагревании капелек несгоревшего топлива и угольных частичек появляется светящийся эффект.
Вторая зона окружена слабозаметной оболочкой с высокими температурными значениями. В нее заходит много кислородных молекул, что способствует полному догоранию топливных частичек. После окисления веществ, в третьей зоне светящийся эффект не наблюдается.
Схематическое изображение
Для наглядности представляем вашему вниманию изображение горения свечи. Схема пламени включает:
- Первую или темную область.
- Вторую светящуюся зону.
- Третью прозрачную оболочку.
Нить свечи не подвергается горению, а только происходит обугливание загнутого конца.

Горение спиртовки
Для химических экспериментов часто используют небольшие резервуары со спиртом. Их называют спиртовками. Фитиль горелки пропитывается залитым через отверстие жидким топливом. Этому способствует давление капиллярное. При достижении свободной верхушки фитиля, спирт начинает испаряться. В парообразном состоянии он поджигается и горит при температуре не более 900 °C.
Пламя спиртовки имеет обычную форму, оно практически бесцветное, с небольшим оттенком голубого. Его зоны не так четко видны, как у свечки.
У спиртовой горелки, названной в честь ученого Бартеля, начало огня располагается над калильной сеткой горелки. Такое заглубление пламени приводит к уменьшению внутреннего темного конуса, а из отверстия выходит средний участок, который считается самым горячим.

Цветовая характеристика
Излучения различных цветов пламени, вызывается электронными переходами. Их еще называют тепловыми. Так, в результате горения углеводородного компонента в воздушной среде, синее пламя обусловлено выделением соединения H-C. А при излучении частичек C-C, факел окрашивается в оранжево-красный цвет.
Трудно рассмотреть строение пламени, химия которого включает соединения воды, углекислого и угарного газа, связь OH. Его языки практически бесцветны, так как вышеуказанные частички при горении выделяют излучения ультрафиолетового и инфракрасного спектра.
Окраска пламени взаимосвязана с температурными показателями, с наличием в нем ионных частиц, которые относятся к определенному эмиссионному или оптическому спектру. Так, горение некоторых элементов приводит к изменению цвета огня в горелке. Отличия в окрашивании факела связаны с расположением элементов в разных группах системы периодической.
Огонь на наличие излучений, относящихся к видимому спектру, изучают спектроскопом. При этом было установлено, что простые вещества из общей подгруппы оказывают и подобное окрашивание пламени. Для наглядности используют горение натрия в качестве теста на данный металл. При внесении его в пламя, языки становятся ярко-желтыми. На основании цветовых характеристик выделяют натриевую линию в эмиссионном спектре.
Для щелочных металлов характерно свойство быстрого возбуждения светового излучения атомарных частиц. При внесении труднолетучих соединений таких элементов в огонь горелки Бунзена происходит его окрашивание.
Спектроскопическое исследование показывает характерные линии в области, видимой для глаза человека. Быстрота возбуждения светового излучения и простое спектральное строение тесно взаимосвязаны с высокой электроположительной характеристикой данных металлов.
Характеристика
В основе классификации пламени лежат следующие характеристики:
- состояние агрегатное сгорающих соединений. Они бывают газообразной, аэродисперсной, твердой и жидкой формы;
- тип излучения, которое может быть бесцветным, светящимся и окрашенным;
- распределительная скорость. Существует быстрое и медленное распространение;
- высота пламени. Строение может быть коротким и длинным;
- характер передвижения реагирующих смесей. Выделяют пульсирующее, ламинарное, турбулентное перемещение;
- визуальное восприятие. Вещества горят с выделением коптящего, цветного или прозрачного пламени;
- температурный показатель. Пламя может быть низкотемпературным, холодным и высокотемпературным.
- состояние фазы топливо – окисляющий реагент.
Возгорание происходит в результате диффузии или при предварительном перемешивании активных компонентов.

Окислительная и восстановительная область
Процесс окисления протекает в слабозаметной зоне. Она самая горячая и располагается вверху. В ней топливные частицы подвергаются полному сгоранию. А наличие в кислородного избытка и горючего недостатка приводит к интенсивному процессу окисления. Этой особенностью следует пользоваться при нагревании предметов над горелкой. Именно поэтому вещество погружают в верхнюю часть пламени. Такое горение протекает намного быстрее.
Восстановительные реакции проходят в центральной и нижней части пламени. Здесь содержится большой запас горючих веществ и малое количество O2 молекул, осуществляющих горение. При внесении в эти области кислородсодержащих соединений осуществляется отщепление O элемента.
В качестве примера восстановительного пламени используют процесс расщепления железа двухвалентного сульфата. При попадании FeSO4 в центральную часть факела горелки, происходит вначале его нагревание, а затем разложение на оксид трехвалентного железа, ангидрид и двуокись серы. В данной реакции наблюдается восстановление S с зарядом от +6 до +4.
Сварочное пламя
Данный вид огня образуется в результате сгорания смеси из газа или пара жидкости с кислородом чистого воздуха.

Примером служит формирование пламени кислородно-ацетиленового. В нем выделяют:
- зону ядра;
- среднюю область восстановления;
- факельную крайнюю зону.
Так горят многие газокислородные смеси. Различия в соотношении ацетилена и окислителя приводят к разному типу пламени. Оно может быть нормального, науглероживающего (ацетиленистого) и окислительного строения.
Теоретически процесс неполного сгорания ацетилена в чистом кислороде можно охарактеризовать следующим уравнением: HCCH + O2 → H2 + CO +CO (для реакции необходима одна моль O2).
Полученный же молекулярный водород и угарный газ реагируют с воздушным кислородом. Конечными продуктами является вода и оксид четырехвалентного углерода. Уравнение выглядит так: CO + CO + H2 + 1½O2 → CO2 + CO2 +H2O. Для этой реакции необходимо 1,5 моля кислорода. При суммировании O2 получается, что 2,5 моль затрачивается на 1 моль HCCH. А так как на практике трудно найти идеально чистый кислород (часто он имеет небольшое загрязнение примесями), то соотношение O2 к HCCH будет 1,10 к 1,20.
Когда значение пропорции кислорода к ацетилену меньше 1,10, возникает науглероживающее пламя. Строение его имеет увеличенное ядро, очертания его становятся расплывчатыми. Из такого огня выделяется копоть, вследствие недостатка кислородных молекул.
Если же соотношение газов больше 1,20, то получается окислительное пламя с кислородным избытком. Лишние его молекулы разрушают атомы железа и другие компоненты стальной горелки. В таком пламени ядерная часть становится короткой и имеет заострения.
Температурные показатели
Каждая зона огня свечи или горелки имеет свои значения, обусловленные поступлением кислородным молекул. Температура открытого пламени в разных его частях колеблется от 300 °C до 1600 °C.
Примером служит пламя диффузионное и ламинарное, которое образовано тремя оболочками. Конус его состоит из темного участка с температурой до 360 °C и недостатком окисляющего вещества. Над ним располагается зона свечения. Ее температурный показатель колеблется от 550 до 850 °C, что способствует разложению термическому горючей смеси и ее горению.
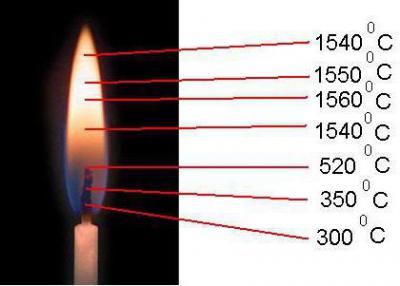
Внешняя область едва заметная. В ней температура пламени доходит до 1560 °C, что обусловлено природными характеристиками топливных молекул и быстротой поступления окисляющего вещества. Здесь горение наиболее энергичное.
Вещества воспламеняются при разных температурных условиях. Так, металлический магний горит только при 2210 °С. Для многих твердых веществ температура пламени около 350 °С. Возгорание спичек и керосина возможно при 800 °С, тогда как древесины – от 850 °С до 950 °С.
Сигарета горит пламенем, температура которого варьируется от 690 до 790 °С, а в пропан-бутановой смеси – от 790 °С до 1960 °С. Бензин воспламеняется при 1350 °С. Пламя горения спирта имеет температуру не более 900 °С.
Какой огонь горячее синий или красный
Если вы откроете кран с синей заглушкой, какой температуры вода из него польётся? А если с красной? Всё верно. Из-за того, что красный цвет традиционно ассоциируется с огнём, а синий — с водой или льдом, красным и синим обычно обозначают температурные полюса «горячий-холодный». Соответственно, велики шансы, что темпераментный и вспыльчивый персонаж будет любить красный цвет и предпочитать его в одежде, тогда как более спокойный и уравновешенный герой предпочтёт голубые или синие оттенки.
В реальной жизни зигзаг:
- горячие звёзды — голубые, а холодные — красные;
- но при этом у красных звёзд изрядная часть излучения лежит в инфракрасном тепловом диапазоне (а также в радиодиапазоне, включая микроволны, способствующие нагреву же, в то время как у голубых звёзд изрядная часть излучения — это рентгеновское и гамма-излучение);
- из-за того, что голубые звёзды светят ярко, а красные — тускло, в итоге выходит, что голубые звёзды греют сильнее красных;
- плюс ко всему кванты света в синем диапазоне обладают большей энергией, чем в диапазоне красном.
А вот ассоциативный ряд выработался потому, что мы (пока что) не галактические суперчудища и не достаточно развитые инопланетяне, которым важно не обжечься об звезду или собрать побольше энергии Сферой Дайсона, и эволюцией всё-таки настроен на такие очень локальные для этой планеты явления, как вода, огонь, грунт и влажные сочные листья (последние два вообще локальны до неприличия).
- Но вполне приземленно — холодное пламя красно-оранжевое, при этом часто еще и коптит, потом желтеет, белеет, голубеет. При дальнейшем росте температуры остается голубым, но начинает тускнеть, т.к. свечение уползает в невидимый ультрафиолет (привет зрителям без маски).
Нетрудно догадаться, что оттенок пламени определяется химическими веществами, сгорающими в нем, в том случае, если воздействие высокой температуры высвобождает отдельные атомы сгораемых веществ, окрашивая огонь. Чтобы определить влияние веществ на цвет огня, проводились различные эксперименты, о которых поговорим ниже.
 С древних времен алхимики и ученые старались узнать, какие вещества сгорают, в зависимости от цвета, который приобретало пламя.
С древних времен алхимики и ученые старались узнать, какие вещества сгорают, в зависимости от цвета, который приобретало пламя.
Пламя газовых колонок и плит, имеющихся во всех домах и квартирах, имеет голубой оттенок. Такой оттенок при сгорании дает углерод, угарный газ. Желто-оранжевый цвет пламени костра, который разводят в лесу, или бытовых спичек, обусловлен высоким содержанием солей натрия в природной древесине. Во многом благодаря этому цвет пожарной машины — красный. Пламя конфорки газовой плиты приобретет тот же цвет, если посыпать ее обыкновенной поваренной солью. При горении меди пламя будет зеленого цвета. Думаю, вы замечали, что при долгой носке кольца или цепочки из обычной меди, не покрытой защитным составом, кожа становится зеленого оттенка. То же самое происходит при процессе горения. Если содержание меди высокое, имеет место очень яркий зеленый огонь, практически идентичный белому. Это можно увидеть, если насыпать на газовую конфорку медной стружки.
Было проведено много экспериментов с участием обыкновенной газовой горелки и различных минералов. Таким образом определялся их состав. Нужно взять минерал пинцетом и поместить в пламя. Цвет, который приобретет огонь, может указать на различные примеси, имеющиеся в элементе. Пламя зеленого цвета и его оттенков говорит о присутствии меди, бария, молибдена, сурьмы, фосфора. Бор дает сине-зеленый цвет. Селен придает пламени синий оттенок. В красный пламя окрашивается при наличии стронция, лития и кальция, в фиолетовый — калия. Желто-оранжевый цвет получается во время горения натрия.
Исследования минералов для определения их состава проводятся с использованием бунзеновской горелки. Цвет ее пламени ровный и бесцветный, он не мешает ходу опыта. Бунзен изобрел горелку в середине XIX века.
Он и придумал метод, позволяющий определить состав вещества по оттенку пламени. Подобные эксперименты ученые пытались проводить и до него, но они не обладали бунзеновской горелкой, бесцветное пламя которой не мешало ходу эксперимента. Он помещал в огонь горелки разные элементы на проволоке из платины, так как при внесении этого металла пламя не окрашивается. На первый взгляд метод кажется хорошим, можно обойтись без трудоемкого химического анализа. Достаточно лишь поднести элемент к огню и увидеть из чего он состоит. Но вещества в чистом виде можно встретить в природе крайне редко. Обычно в них в большом количестве содержатся различные примеси, которые изменяют окраску пламени.
Бунзен пытался выделить цвета и оттенки различными методами. К примеру, с помощью цветных стекол. Допустим, если смотреть через синее стекло, не будет виден желтый цвет, в который огонь окрашивается при горении наиболее часто встречающихся солей натрия. Тогда становится различимым лиловый или малиновый оттенок искомого элемента. Но даже такие ухищрения приводили к верному определению состава сложного минерала в очень редких случаях. Большего такая технология не смогла добиться.
В наши дни такую горелку используют только для пайки.

Пламя бывает разного цвета. Посмотрите в камин. На поленьях пляшут желтые, оранжевые, красные, белые и синие языки пламени. Его цвет зависит от температуры горения и от горючего материала. Чтобы наглядно себе это представить, вообразите спираль электрической плитки. Если плитка выключена — витки спирали холодные и черные. Допустим, вы решили подогреть суп и включили плитку. Сначала спираль становится темно-красной. Чем выше поднимается температура, тем ярче красный цвет спирали. Когда плитка разогревается до максимальной температуры, спираль становится оранжево-красной.
Естественно, спираль не горит. Вы же не видите пламени. Она просто очень горячая. Если нагревать ее дальше, то будет меняться и цвет. Сначала цвет спирали станет желтым, затем белым, а когда она раскалится еще больше, от нее будет исходить голубое сияние.

Нечто подобное происходит и с пламенем. Возьмем для примера свечу. Различные участки пламени свечи имеют разную температуру. Огню нужен кислород. Если свечу накрыть стеклянной банкой, огонь погаснет. Центральный, прилегающий к фитилю участок пламени свечи, потребляет мало кислорода, и выглядит темным. Верхушке и боковым участкам пламени достается больше кислорода, поэтому эти участки ярче. По мере того как пламя продвигается по фитилю, воск тает и потрескивает, рассыпаясь на мельчайшие частички углерода. (Каменный уголь тоже состоит из углерода.) Эти частички увлекаются пламенем кверху и сгорают. Они очень горячие и светятся, как спираль вашей плитки. Но частички углерода намного горячее, чем спираль самой жаркой плитки (температура сгорания углерода примерно 1 400 градусов Цельсия). Поэтому свечение их имеет желтый цвет. Около горящего фитиля пламя еще горячее и светится синим цветом.
Пламя камина или костра в основном пестрого вида. Дерево горит при более низкой температуре, чем фитиль свечи, поэтому основной цвет костра — оранжевый, а не желтый. Некоторые частички углерода в пламени костра имеют довольно высокую температуру. Их немного, но они добавляют пламени желтоватый оттенок. Остывшие частички раскаленного углерода — это копоть, которая оседает на печных трубах. Температура горения дерева ниже температуры горения свечи. Кальций, натрий и медь, нагретые до высокой температуры, светятся разными цветами. Их добавляют в порох ракет для расцвечивания огней праздничных фейерверков.
Цвет пламени и химический состав
Цвет пламени может меняться в зависимости от химических примесей, содержащихся в поленьях или другом горючем веществе. В пламени может находиться, например, примесь натрия.

Еще в древние времена ученые и алхимики пытались понять, что за вещества сгорают в огне, в зависимости от того, в какой цвет окрашивался огонь.
- Натрий — это составная часть поваренной соли. Если натрий раскалить, он окрашивается в ярко — желтый цвет.
- В огонь может попасть кальций. Мы все знаем, что кальция много в молоке. Это металл. Раскаленный кальций окрашивается в яркий красный цвет.
- Если в огне горит фосфор, то пламя окрасится в зеленоватый цвет. Все эти элементы или содержатся в дереве, или попадают в огонь с другими веществами.
- Практически у всех дома есть газовые плиты или колонки, пламя в которых окрашено в голубой оттенок. Это обусловлено сгораемым углеродом, угарным газом, который и дает этот оттенок.

Смешение цветов пламени, как и смешение цветов радуги, может дать белый цвет, поэтому в пламени костра или камина видны белые участки.
Температура пламени при горении некоторых веществ:
Почему газ горит красным пламенем на плите: факторы влияющие на цвет пламени

Со временем пользования газовой плитой многие замечают, как цвет пламени меняется с голубого на какой-то другой. Возникает вопрос: каким цветом должен быть газ на плите при нормальной работе оборудования? Нормально ли, что он горит не синим, а каким-то другим цветом? И в каких случаях изменение цвета пламени указывает на серьезные проблемы.
Действительно, изменение окраски пламени практически всегда указывает на проблемы. Но большинство из них вполне можно решить самостоятельно и даже не вызывать специальные службы. Рассмотрим почему газ горит иногда оранжевым, а не синим пламенем, и как эту проблему устранить.
Причины изменения цвета пламени
Газовое оборудование относится к небезопасным бытовым приборам. С одной стороны, пользователь не должен вмешиваться в его работу и нарушать конструкцию плиты, пытаться отремонтировать ее самостоятельно.
С другой – важно знать возможные признаки поломок и вовремя на них реагировать, чтобы не эксплуатировать варочную поверхность, которая вышла из строя.

Один из самых простых признаков проблем в работе плиты является изменение окраски огня. В норме он синий, но иногда может становиться оранжевым, красным, желтым, иметь резкий и неприятный запах.
Важное условие для нормального сжигания газа – необходимое количество кислорода. Существует определенная пропорция, которую необходимо соблюдать, чтобы горение было максимально полезным для пользователя.
Причины изменения цвета пламени:
- неполное сгорание газа;
- неправильное количество воздуха в смеси (недостаточное или избыточное);
- загрязненность конфорок;
- неподходящее оборудование;
- некачественный газ.
Бытует мнение, что изменение цвета газа указывает на плохое качество поставляемого топлива. Якобы его разбавляют различными веществами, чтобы потребитель платил больше за услугу. На самом же деле, цвет огня указывает только на то, насколько правильно осуществляется процесс сгорания.
Так, однородный голубой цвет свидетельствует о полном сгорании газа с извлечением максимального количества тепла.

Но нельзя исключать и поставку некачественного газа. На сам цвет горения это не влияет, но некачественный газ в будущем ухудшает работу плиты и приводит к появлению желтого цвета пламени.
После работы плиты на ней может собираться черная сажа. Все это свидетельствует о том, что пламя коптит. Это указывает на нарушение инжекции газа. При работе конфорок ощущается нехватка газовой смеси. Вот почему газ иногда горит красным или желтым пламенем на плите.
Нужно искать причину прежде всего в загрязнении горелок, проблемах с вентиляцией и т. д. Чем выше температура горения, то есть, чем больше насыщен газ кислородом при горении, тем более холодный оттенок пламени.
Желтая окраска пламени
Топливовоздушная смесь становится непригодной и меняет свой цвет по разным причинам. Наиболее частая – забиваются отверстия, предназначенные для всасывания воздуха. В них попадает пыль, которая препятствует свободному проходу воздуха.
Особенно эта проблема актуальна в первые годы пользования газовым оборудованием. Именно тогда нужно чаще всего подвергать его проверке. Связано это с тем, что после штамповки на горелке и трубке запальной группы первое время сохраняется небольшая масляная пленка. Это приводит к налипанию пыли на ее поверхность, что препятствует попаданию нормального количества воздуха. Газ при этом проходит в прежнем количестве.
Меняется состав смеси, и это становится причиной, почему газ горит оранжевым или желтым цветом в плите, а не традиционным голубым или синим.

Важно понимать, что изменение окраски пламени – не единственный признак того, что плиту пора почистить.
Другие показатели следующие:
- пламя коптит;
- огонь приобретает непрозрачный оттенок;
- факел становится слишком большим;
- факел становится светящимся.
Это все указывает на необходимость вызывать мастера, чтобы он почистил горелки, их различные элементы и отрегулировал работу плиты, чтобы воздух подавался равномерно.
Еще одна частая причина изменения цвета газового пламени на желтый – пребывание заслонки для регулирования подачи воздуха в неправильном положении. Она может быть закрытой, соскочить, упасть и т. д. Это вызывает недостаток воздуха, что приводит к потере нагрева, появлению копоти, желтому пламени и других проблем. Нередко это заканчивается даже необходимостью делать срочный ремонт плиты.
Пламя горит красным
Иногда газ может гореть даже красным цветом. Причиной такого явления служит избыток угарного газа, который накапливается как побочный продукт горения любого топлива. Если газ горит синим пламенем, значит, газовое оборудование полностью исправно и выделяет небольшое количество угарного газа.
Если же цвет меняется ближе к красному – этого ядовитого вещества становится все больше. Это довольно опасно, ведь чрезмерная концентрация приводит к головной боли, тошноте, головокружению и другим признакам отравления.

Проблема угарного газа в том, что он без запаха и цвета. Поэтому окраска пламени – единственный способ распознать увеличение его концентрации.
Даже небольшие концентрации этого вещества (0,01-0,2%) приводят к тяжелым симптомам.

Если концентрация газа достигнет больших величин, то это может вызвать более серьезные отравления и даже летальный исход.
Каким цветом должен гореть газ?
Итак, чтобы происходило максимально полное сгорание газа и при этом выделялось нужное количество энергии, важно, чтобы в газовой смеси было достаточно воздуха. Это достигается благодаря смешению кислорода и горящего газа в горелке в нужных пропорциях: на 1 литр горящего газа необходимо 10 литров воздуха.
Тогда сковорода или кастрюля будет нагреваться достаточно быстро, ведь из конфорки будет выделяться много тепла. Полное сгорание газа обеспечивает нормальное выделение тепла, некоторого количества света при образовании углекислого газа и паров воды.
Об этом свидетельствуют такие признаки:
- бесшумное горение газа;
- синий цвет пламени;
- равномерное распределение пламени по всем сторонам конфорки;
- достаточный уровень огня;
- поджиг без хлопков;
- нет прекращения горения на минимальном значении регулятора мощности пламени.
Если же возникают какие-то препятствия для попадания воздуха, сгорание газа происходит неполноценно. Окисление в недостаточном присутствии воздуха приводит к образованию окиси углерода (или угарного газа), из-за чего цвет меняется на желтый или даже красный.

Если же в горелку поступает слишком много природного газа, начинается неправильный расход топлива, что вызывает образование копоти в горелке. Падает нагрев,что приводит к увеличению длительности приготовления пищи, а на нижней стороне посуды начинают появляться черные следы после нахождения на газовой плите. Все это указывает на проблемы в работе газовой конфорки и на необходимость срочной ее чистки.
Также рекомендуем прочесть другие наши каналы, где мы подробно рассказали о возможных проблемах с газовыми конфорками и способах их решения:
Устранение проблем с изменением цвета
Самая распространенная ошибка, которую часто допускают пользователи газового оборудования – приобретение неподходящего оборудования.
Некоторые изделия подходят только для одного вида газа, а в использовании может быть другой. Тогда возможно также изменение цвета пламени.

Например, бытовой прибор может работать на пропане. Для него нужна несколько иная пропорция газа и воздуха, чем для природного газа. Поэтому перед приобретением плиты важно поинтересоваться, для той ли газовой смеси она предназначена, которую использовать будете вы.
Итак, если цвет газового пламени поменялся на желтый, оранжевый или красный, прежде всего, необходимо признать наличие опасности. Многие начинают списывать все на некачественный газ, на проблемы у поставщика, но чаще всего причина именно в самих конфорках.
Важно найти источник изменения цвета и устранить его неполадки. Если вы это не можете сделать самостоятельно, рекомендуется обратиться в компанию, с которой у вас заключен договор на ТО газового оборудования. Они проведут диагностику, выполнят ремонт устройства в случае необходимости.

Важно также выполнять профилактические меры. Чаще всего газ меняет свой цвет из-за того, что конфорки внутри засоряются бытовой пылью, остатками еды. Если более аккуратно пользоваться плитой, делать регулярную уборку, можно избежать попадания ненужных предметов внутрь горелки. Это усилия, которые может приложить абсолютно каждый пользователь.
Очищение можно выполнять с использованием специальных моющих средств. Делать это нужно, когда конфорки полностью остыли.
Старайтесь выполнять такие правила очистки:
- эмалированные и металлические поверхности очищайте без использования абразивных чистящих средств;
- не используйте хлорсодержащие очистители;
- поверхности из стеклокерамики очищайте мыльным раствором;
- для самих отверстий используйте щетку с жесткой щетиной.
В заключении протирают сухой тряпкой очищенную плиту, ждут, пока она высохнет, и пробуют зажечь газ.
Если очистка конфорок не исправила ситуацию, и газ, по-прежнему, оранжевого цвета, то здесь выход только один. Сразу же нужно обратиться в специализированный сервисный центр, который занимается ремонтом газового оборудования.

Если вы не знаете, как их разобрать и почистить, можно заглянуть в инструкцию к своей газовой плите. Там должны быть описаны способы очистки этих механизмов. Кроме того, важно держать в чистоте всю плиту, даже самые удаленные ее части от огня. Ведь в некоторых случаях загрязнения с тех мест могут случайно переноситься и попадать под заслонку.
Большинство из описываемых выше рекомендаций могут показаться на первый взгляд элементарными и несерьезными. Многие думают, что нормально обращаются со своей плитой и контролируют ситуацию. На самом деле, внутри плиты могут происходить совершенно иные процессы.
Пыль, которую вы не убрали сразу, потом попадает внутрь горелки, где оплавляется и обугливается. И в таком случае ее весьма сложно становится очистить. И если бытовой прибор продолжать эксплуатировать в таком духе, его состояние будет ухудшаться все больше и больше. В конечном итоге, это приведет к полному выходу из строя.
Не затягивайте с обращением в газовые службы и к специалистам. Если плита систематически работает со сбоями, ей нужен ремонт. Полезными будут также профилактические осмотры от специалистов.
Кроме того, не следует пренебрегать правилами безопасной эксплуатации газового оборудования, ведь даже малейшая ошибка может привести к печальным последствиям.
Выводы и полезное видео по теме
Не всегда можно с первого раза разобраться, как почистить газовую конфорку от накипи и грязи. В видео ниже предлагается подробная инструкция, как это сделать:
Итак, нормальный цвет газового пламени – синий. Если же ваши конфорки горят по-другому, это повод их почистить или вызвать специалиста для более полной диагностики. Не стоит затягивать с этим вопросом, ведь меняется не просто цвет пламени, а состав продуктов горения.
Накопление угарного газа может привести к нежелательным последствиям. Поэтому вопросы газовой безопасности необходимо решать в первую очередь.
Приходилось ли вам сталкиваться с изменением цвета пламени? Как вы действовали в такой ситуации? Оставляйте свои комментарии, делитесь опытом, задавайте вопросы – блок для связи расположен под статьей.


