Где встречается железо в природе
Железо в природе (4,7% в Земной коре)
 Железо стоит на втором месте (4,7% в Земной коре) после алюминия по запасам и распространенности на планете. Оно обнаружено еще на заре человеческого общества и до сих пор не теряет своего значения и повсюду используется.
Железо стоит на втором месте (4,7% в Земной коре) после алюминия по запасам и распространенности на планете. Оно обнаружено еще на заре человеческого общества и до сих пор не теряет своего значения и повсюду используется.
Чаще всего железо находят в богатых металлом рудах, которые можно относительно легко добывать и перерабатывать. В чистом виде железо находили только в метеоритах, а в соединениях оно присутствует в сульфидах, силикатах и оксидах.
Характеристика железа
Физические свойства

Железо – это серебристо-белый металл с сероватым оттенком. В чистом виде пластичен, но непрочен. При добавлении в него различных добавок (например, углерода) твердость и хрупкость сплава повышается. Железо хорошо проводит электричество, тепло и обладает мощными магнитными свойствами, то есть под действием магнитного поля оно намагничивается и потом само становится магнитом.
Железо особенно важно для живых организмов. Оно способствует дыхательным процессам и входит в состав гемоглобина крови (477 мг/л). Это значит, что железо участвует в процессе доставки кислорода от органов дыхания к тканям.
Находясь в воде и на влажном воздухе железо меркнет и ржавеет, а при температуре 1539°С легко плавится и поддается ковке. При высоких температурах железо реагирует с паром воды.
Железо образует 300 разнообразных минералов (карбонаты, сульфиды и т.д.) и энергично мигрирует в земной коре. Его называют металлом земных недр, так как он копится в кристаллизации магмы.
Химические свойства

Железо — металл со средней степенью химической активности. На воздухе, на нем образуется защитная пленка, которая препятствует коррозии и ржавлению. Если воздух влажный, железо окисляется и покрывается ржавчиной.
Растворяется в разведенной соляной или серной кислотах, с выделением водорода. Вытесняет из растворов солей металлы. Во время нагревания взаимодействует с неметаллами.
Соединения и нахождение железа в природе

В естественных водах, среднее содержание железа (в интервале 0,01-26 мг/л). Кроме того, животные особи, бактерии и растения содержат его в своих организмах. Даже в тканях и внутренних органах людей есть железо, поступающее в организм вместе с едой. Потребность в нем для взрослого человека составляет 11-30мг. Избыток железа приводит к гемохроматозу и серьезным нарушениям внутренних органов.
Так как месторождения железных руд возникают в разных геологических условиях, то и состав руд и условия их расположения разнообразны.
Железо содержится во многих рудах:
• гематит (железный блеск, красный железняк),
• пирит (серный колчедан) и гетит,
• магнетит (магнитный железняк),
• сидерит и гидрогенит.
Круговорот железа в природе
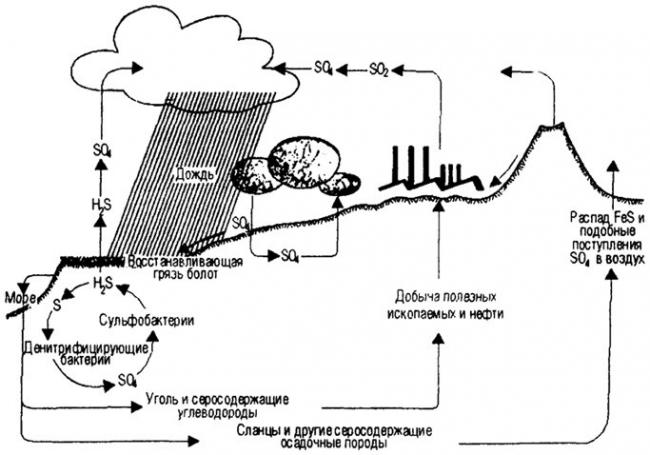
(На примере круговорота серы и других соединений в природе)
За счет жизнедеятельности железобактерий (нитевидные бактерии и одиночные железобактерии) происходит круговорот железа в природе. Они окисляют железо до гидроксида железа, а углерод получают из углекислоты. Таким образом, железобактерии получают энергию для своей жизнедеятельности, а после смерти осаждаются в почве в виде болотной руды.
Области применения железа
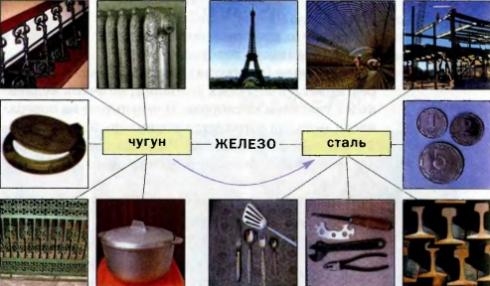
В чистом виде железо непрочно, поэтому практически не применяется. Его используют для выработки электромагнитов, как катализатор химических реакций и др.
Основное применение этот металл находит в виде сплавов. На их долю приходится 95% всей металлопродукции. Железо основной компонент стали и чугуна. В стали меньше углерода, чем в чугуне, и поэтому она более пластична и устойчива к резким ударным нагрузкам железа.
Так же железо входит в состав никелевых и других сплавов, использующихся в электротехнике, железо-воздушных аккумуляторах и железо — никелевых аккумуляторах.
На основе железа производятся материалы, которые могут выдерживать действие низкой и повышенной температуры, агрессивной среды, ядерных излучений, вакуума и высоких давлений и т. п.
Железо относится к группе тех металлов, которые очень широко применяются во всех областях народного и бытового хозяйства. Чугун и сталь стали основой современной техники. С их участием произошло развитие тяжелой промышленности, разнообразного наземного транспорта и др.
Большие запасы железа в России, Австралии, Канаде, Казахстане, Индии, Франции, США, Венесуэле и ЮАР.
Круговорот железа в природе. Железобактерии. Добыча и области применения железа
Что это такое — железо, откуда оно взялось и как его добывают? Этот полезный металл имеет множество областей применения. Химический элемент играет важную роль в мировой промышленности, а важное значение в жизни планеты имеет круговорот железа в природе.

Что такое железо?
Железо представляет собой металлический элемент, который является очень химически реактивным, особенно когда он взаимодействует с кислородом. Это один из наиболее распространенных элементов на Земле и в космосе. Атомы железа содержат 26 протонов в своих ядрах. Химический символ — Fe (ферум) происходит от его латинского названия ferum. В чистом виде это мягкий и хрупкий металл, который усиливается при помощи примесей. При соединении с углеродом получается сталь, для производства которой используется более 98 % добываемой сегодня железной руды.

Все атомы железа во Вселенной образовались в ядрах звезд на заключительных этапах слияния, а затем были выпущены в космос путем звездных взрывов. Это четвертый по численности элемент в земной коре после кремния, кислорода и алюминия. Что такое железо? Это самый распространенный элемент, составляющий нашу планету, хотя большая его часть по массе находится намного ниже поверхности — в ядре Земли. Он присутствует почти во всех породах коры и мантии в качестве химического компонента сотен различных минералов.

Железная руда
В чистом виде этот металл встречается редко. Некоторые метеориты содержат элементарное железо. Этот элемент химически реагирует с кислородом и водой для производства железосодержащих минералов. Любой камень, который содержит достаточное количество этого металла, добываемого в экономических целях, называется железной рудой. Наиболее распространенными ее минералами являются:
- оксид железа (формула Fe2O3), который образуется под воздействием кислорода;
- гидратированный оксид железа, который образуется в результате реакции в воде.
Наиболее важными железными рудами являются минералы оксида железа, называемые гематитом и магнетитом. Высокая концентрация Fe делает их наиболее предпочтительными в промышленности. Добыча железа осуществляется на крупнейших месторождениях руды. Чаще всего это образования, которые представляют собой древние осадочные породы. Они содержат слои минералов оксида железа (формула Fe2O3) толщиной до нескольких сантиметров.

Где можно найти железо?
При комнатной температуре оно представляет собой твердое вещество. Это блестящий серый металл, который ржавеет со временем при воздействии влажного воздуха. Он объединяется со многими другими металлами для образования сплавов. Области применения железа достаточно обширные. Когда он сочетается с углеродом, получается сталь. Его также можно комбинировать с другими металлами, такими как никель, хром и вольфрам. Эти сплавы очень прочные и могут использоваться для изготовления мостов и зданий.
Железо — очень древний элемент, который использовался на Земле в течение долгого времени. Объекты из него были найдены еще в Древнем Египте. Был даже целый период времени (1200-500 гг. до н. э.), названный в его честь, — железный век, когда его использовали для изготовления орудий и оружия. Чтобы найти этот полезный металл, нужно искать его глубоко под землей. Он встречается как в земной коре, так и в ядре Земли. На Земле железа больше, чем любого другого металла. Этот элемент можно найти и на других планетах, включая ядро Юпитера и Сатурна, а также красную пыльную поверхность Марса (именно в связи с этим его и назвали Красной планетой).

Наземный круговорот железа в природе
Железо (Fe) следует за геохимическим циклом, как и многие другие питательные вещества. Оно обычно выделяется в почву или в океан через выветривание горных пород или извержения вулканов. В земной экосистеме растения сначала поглощают железо через корни из почвы. Это предельно важное питательное вещество, которое перемещается между живыми организмами и геосферой.
Железо является важным ограничивающим питательным веществом для растений, которые используют его для производства хлорофилла. Фотосинтез зависит от адекватного снабжения этим металлом. Растения ассимилируют его из почвы в корни. Животные потребляют растения и используют его для производства гемоглобина. Когда они умирают, они разлагаются и бактерии возвращают металл в почву.

Морской цикл железа
Морской круговорот железа в природе очень похож на земной цикл. Этот процесс происходит за счет жизнедеятельности определенных микроорганизмов, окисляющих металл до гидроксида и получающих углерод из углекислоты. Железобактерии в реке, море или любом другом водоеме добывают энергию для своего жизненного цикла, а после его завершения они оседают в почве в виде болотной руды.
Роль железа в океанических экосистемах также значительная. Основными производителями, которые поглощают этот металл, обычно являются фитопланктон или цианобактерии. Затем железо усваивается потребителями, когда они едят эти бактерии. Круговорот железа в природе — это чрезвычайно сложный процесс. Он зависит от множества сопутствующих факторов: химических реакций, типов мест обитания и групп микробов. Все это связывает его с другими, не менее важными биогеохимическими циклами Земли.

Общая характеристика
Железо в виде различных комбинированных руд является одним из наиболее распространенных элементов, составляющих около 5 % земной коры. Важнейшими железосодержащими минералами являются оксиды и сульфиды (гематит, магнетит, гетит, пирит, марказит). Этот металл присутствует также в метеоритах, на других планетах и на солнце. Железо содержится как в морской, так и в пресной воде.

Интересные факты
Вот некоторые интересные факты о таком, казалось бы, простом химическом элементе:
- Железо — это важнейший строительный блок для питания растений, который помогает переносить кислород в крови, тем самым поддерживая жизнь на Земле.
- Это хрупкое твердое вещество, классифицированное как металл в группе 8 в периодической таблице элементов. Он в чистом виде быстро корродирует от воздействия влажного воздуха и высоких температур.
- Это четвертый наиболее распространенный элемент земной коры по весу, и большая часть ядра Земли, как полагают, состоит из железа.
- Большая часть его используется для производства стали — сплава железа и углерода, который, в свою очередь, применяется в производстве и строительстве, например для производства железобетона.
- Нержавеющая сталь, содержащая не менее 10,5 % хрома, обладает высокой устойчивостью к коррозии. Она используется в кухонных столовых приборах и посуде, таких как кастрюли из нержавеющей стали.
- Добавление других элементов может обеспечить стали новые полезные свойства. Например, никель увеличивает долговечность сплава и делает его более устойчивым к нагреву и кислотам.

- Число протонов в ядре: 26.
- Атомный символ: Fe.
- Средняя масса атома: 55,845 г/моль.
- Плотность: 7,874 грамма на кубический сантиметр.
- Фаза при комнатной температуре: сплошная.
- Точка плавления: 1538 0 C.
- Точка кипения: 2861 0 C.
- Количество изотопов: 33.
- Стабильные изотопы: 4.
Основные области применения
Железо используется во многих секторах, таких как электроника, производство, автомобилестроение и строительство. Ниже приведены области применения железа:
- В качестве первичной составляющей черных металлов, сплавов и стали.
- Сплав с использованием углерода, никеля, хрома и различных других элементов для получения чугуна или стали.
- В магнитах.
- В готовых металлических изделиях.
- В промышленном оборудовании.
- В транспортном оборудовании.
- В инструментах.
- В игрушках и спортивных товарах.
Железо составляет 5 % земной коры и является одним из самых распространенных и наиболее используемых металлов. Этот элемент также содержится в мясе, картофеле и овощах и имеет важное значение для животных и людей. Это неотъемлемая часть гемоглобина. Металл является сероватым по внешнему виду и очень пластичным и ковким. Он легко растворяется в разбавленных кислотах и химически активен. Основными районами добычи железа являются Китай, Австралия, Бразилия, Россия и Украина.
Справочник химика 21
Химия и химическая технология
Железо. Нахождение в природе
Нахождение в природе и получение железа, кобальта и никеля [c.136]
Нахождение в природе. Железо является одним из очень распространенных элементов. Содержание его в земной коре достигает 5,1 вес. %. [c.347]
Нахождение в природе и получение в свободном виде. Железо — один из наиболее распространенных металлов. Его содержание в земной коре 4—5 масс.%. В природе встречается в виде минера- [c.375]
Нахождение в природе. В земной коре содержится 0,0016% свинца. Основным минералом свинца является галенит (свинцовый блеск) РЬ5,. которому сопутствуют сульфиды меди, железа, серебра, цинка. Сульфидное сырье перерабатывается комплексно. Источником промышленного добывания свинца является свинцово-цинковые полиметаллические-руды. [c.113]
При оценке роли компонентов среды в процессе растворения металла необходимо принимать во внимание, что его поверхность обычно энергетически неоднородна, т.е. адсорбция даже одной и той же частицы на одних участках поверхности может быть стимулирующей, а на других — ингибирующей. То же относится и к частицам разной природы при их совместном нахождении в растворе. Существенно при этом, что прочность связи адсорбированной частицы с металлом, а, следовательно, и производимый ею эффект, зависит от потенциала. Это, в частности, может приводить к отклонению кривой Е — lgг, характеризующей электрохимическое поведение металла, от обычной прямолинейной зависимости, что наблюдается, например, при растворении железа в солянокислых растворах. Стимулирующая адсорбция — процесс очень быстрый по сравнению с адсорбцией ингибирующей. [c.97]
Нахождение в природе и получение. Железо — один из самых распространенных элементов. В свободном виде оно встречается только в метеоритах совместно с никелем. Соединения его содержатся почти во всех горных породах и почве. [c.174]
Нахождение в природе. Железо встречается в виде магнитного железняка Ре,О, гематита Ре Оз , бурого железняка 2Ре,0, ЗН,0 железного шпата (сидерита) РеСО, железного колчедана (пирита) РеЗ . [c.122]
Однако для изучения природы систем водород — металл термодинамические и кинетические характеристики оказываются недостаточными. Это, очевидно, связано с особым состоянием водорода в металлах. Здесь нет необходимости останавливаться на возможности образования экзотермических и эндотермических растворов водорода в разных металлах. Более тонкие эффекты, заключающиеся в видимом многообразии форм нахождения водорода в одном и том же металле (удаление водорода из металла по частям при комнатной температуре, при нагреве в вакууме и при плавлении в вакууме), электроперенос водорода как к аноду, так и к катоду в сплавах железа [1] ставят нас перед необходимостью изыскания, наряду с тривиальным определением термодинамических и кинетических характеристик систем водород — металл, новых методов исследования этих систем. Естественным этапом в изыскании таких методов является исследование влияния внешнего воздействия на систему, и в качестве способа внешнего воздействия, очевидно, можно избрать наложение электрического поля. [c.49]
Железо (Ferrum). Нахождение в природе. Железо—самый распространенный после алюминия металл на земном шаре о но [c.670]
Природные ресурсы.. Железо — четвертый (после О, Si, AI) по раснростэанениости в земной коре элемент (4,65%). Иногда встречается в природе в свободном состоянии. Это главным обра-вом, железо метеоритного происхождения. Железные метеориты содержат в среднем 90% Fe. 8.5% Ni 0,5 /о Со. На 20 каменных метеоритов приходится в срёднем один железный. Масса метеоритов иногда бывает значительной (сотни и более килограмм). Нахождение железных метеоритов, являющихся осколками небесных тел, дает основания предполагать, что центральная часть земного шара также состоит из железа. Иногда встречается самородное Железо земного происхождения, вынесенное из недр земли расплавленной магмой. [c.554]
Железо (Ferrum). Нахождение в природе. Железо — самый распространенный после алюминия металл на земном шаре оно составляет 4% (масс.) земной коры. Встречается железо в виде различных соединений [c.522]
Нахождение в природе и получение в свободном виде. Марганец относится к довольно распространенным элементам и его содержание в земной коре определяется в 8 10 % (мае.). Он активен и встречается только в виде соединений пиролюзит МпОд, браунит МпзОд, гаусманит МП3О4, марганцовый шпат (родохрозит) МпСОз, родонит Мп810з, марганцевый блеск Мп8. Марганец часто сопутствует железу в его природных соединениях. [c.351]
Нахождение в природе и получение в свободном виде. Железо — один из наиболее распространенных металлов. Его содержание в земной коре 4—5% (мае.). В природе встречается в виде минералов — руд магнетит, или магнитный железняк Есз04 гематит, или красный железняк ЕсаОз гетит, или бурый железняк ЕсзОз-НгО сидерит, или шпатовый железняк РеСОз пирит, или железный колчедан РеЗз, входяш,ий также в сернистые руды других металлов. В СССР имеются крупные месторождения железных руд — Керчь, Урал, Кривой Рог, Курская магнитная аномалия и др. [c.362]
Нахождение е природе. В земной коре содержится 0,0015% 2и в основном в виде сульфида 2п8—цинковой обманки, или сфалерита. В этом минерале цинковых руд цинку всегда сопутствует значительное количество железа, изоморфно его замещающего, а такл Смотреть страницы где упоминается термин Железо. Нахождение в природе: [c.540] [c.365] [c.30] [c.147] [c.243] [c.265] [c.551] [c.587] [c.636] [c.73] [c.221] [c.239] [c.56] [c.197] [c.108] [c.56] [c.200] Смотреть главы в:
Химические и физические свойства железа, применение
Одним из наиболее распространенных металлов в земной коре после алюминия считается железо. Физические и химические свойства его таковы, что оно обладает отличной электропроводностью, теплопроводностью и ковкостью, имеет серебристо-белый цвет и высокую химическую реакционную способность быстро коррозировать при высокой влажности воздуха или больших температурах. Находясь в мелкодисперсном состоянии, оно в чистом кислороде горит и самовоспламеняется на воздухе.
Начало истории железа
В третьем тысячелетии до н. э. люди стали добывать и научились обрабатывать бронзу и медь. Широкого применения из-за дороговизны они не получили. Продолжались поиски нового металла. История железа началась в первом веке до н. э. В природе его можно встретить только в виде соединений с кислородом. Для получения чистого металла необходимо отделить последний элемент. Расплавить железо долго не удавалось, так как его надо было нагреть до 1539 градусов. И только с появлением сыродутных печей в первом тысячелетии до новой эры стали получать этот металл. На первых порах он был хрупким, содержал много шлаков.

Железо в природе
Одного алюминия в литосфере содержится больше, чем железа. В природе его можно встретить только в виде соединений. Трехвалентное железо, вступая в реакцию, окрашивает почву в бурый цвет и придает песку желтоватый оттенок. Оксиды и сульфиды железа разбросаны в земной коре, иногда наблюдаются скопления минералов, из которых впоследствии и добывают металл. Содержание двухвалентного железа в некоторых минеральных источниках придает воде особый привкус.

Какими физическими свойствами железо обладает?
Это пластичный серебристо-белого цвета металл с сероватым оттенком, имеющий металлический блеск. Он является хорошим проводником электрического тока и теплоты. Благодаря пластичности он прекрасно поддается ковке и прокатке. Железо не растворяется в воде, но разжижается в ртути, плавится при температуре 1539 и кипит при 2862 градусов по Цельсию, имеет плотность 7,9 г/см³. Особенностью физических свойств железа является то, что металл притягивается магнитом и после аннулирования внешнего магнитного поля хранит намагниченность. Используя эти свойства его можно применять для изготовления магнитов.
Химические свойства
Железо обладает следующими свойствами:
- на воздухе и в воде легко окисляется, покрываясь ржавчиной;
- в кислороде накаленная проволока горит (при этом образуется окалина в виде оксида железа);
- при температуре 700–900 градусов по Цельсию вступает в реакцию с парами воды;
- при нагревании реагирует с неметаллами (хлором, серой, бромом);
- вступает в реакции с разбавленными кислотами, в результате получаются соли железа и водород;
- не растворяется в щелочах;
- способно вытеснить металлы из растворов их солей (железный гвоздь, в растворе медного купороса, покрывается красным налетом, — это выделяется медь);
- в концентрированных щелочах при кипячении проявляется амфотерность железа.
Особенность свойств
Одним из физических свойств железа является ферромагнитность. На практике с магнитными свойствами этого материала приходится встречаться часто. Это — единственный металл, который обладает такой редкостной чертой.

Запасы и добыча
Одним из самых распространенных элементов на земле является железо. По содержанию в земной коре занимает четвертое место. Известно множество руд, которые содержат его, например, магнитный и бурый железняк. Металл в промышленности получают в основном из руд гематита и магнетита при помощи доменного процесса. Вначале происходит его восстановление углеродом в печи при высокой температуре 2000 градусов по Цельсию.

Преимущества железа
Основные физические свойства вещества железа дают ему и сплавам следующие преимущества перед другими металлами:
- Обладают твердостью и прочностью, сохраняя упругость. У разных сплавов эти качества неодинаковы и зависят от легирующих добавок, способов производства и термообработки.
- Большое разнообразие чугуна и сталей позволяют использовать их для любых нужд в народном хозяйстве.
- Высокие магнитные свойства металла незаменимы для изготовления магнитопроводов.

Недостатки
Кроме большого числа положительных качеств, есть и ряд отрицательных свойств металла:
- Изделия подвержены коррозии. Для устранения этого нежелательного эффекта с помощью легирования получают нержавеющие стали, а в остальных случаях делают специальную антикоррозийную обработку конструкций и деталей.
- Железо накапливает статическое электричество, поэтому изделия, содержащие его, подвергаются электрохимической коррозии и также требуют дополнительной обработки.
- Удельный вес металла составляет 7,13 г/см³. Это физическое свойство железа придает конструкциям и деталям повышенный вес.
Состав и структура
У железа по кристаллическому признаку есть четыре модификации, которые отличаются структурой и параметрами решетки. Для выплавки сплавов именно наличие фазовых переходов и легирующих добавок имеет существенное значение. Различают следующие состояния:
- Альфа-фаза. Она сохраняется до 769 градусов по Цельсию. В этом состоянии железо сохраняет свойства ферромагнетика и обладает объемно-центрированной решеткой кубического типа.
- Бета-фаза. Существует при температуре от 769 до 917 градусов по Цельсию. Имеет немного другие параметры решетки, чем в первом случае. Все физические свойства железа остаются прежними за исключением магнитных, их оно утрачивает.
- Гамма-фаза. Строение решетки становится гранецентрированным. Такая фаза проявляется в диапазоне 917–1394 градусов Цельсия.
- Омега-фаза. Такое состояние металла появляется при температуре выше 1394 градусов Цельсия. От прежней отличается только параметрами решетки.

Применение
Люди начали использовать сначала метеоритное железо, которое ценили выше золота. С тех пор область применения этого металла только расширялась. Ниже представлено применение железа, на основе его физических свойств:
- ферромагнитные оксиды используют для производства магнитных материалов: промышленных установок, холодильников, сувениров;
- оксиды железа применяют как минеральные краски;
- хлорид железа незаменим в радиолюбительской практике;
- сульфаты железа используют в текстильной промышленности;
- магнитная окись железа – один из важных материалов для производства устройств долговременной компьютерной памяти;
- ультрадисперсный порошок железа находит применение в черно-белых лазерных принтерах;
- прочность металла позволяет изготовлять оружие и броню;
- износостойкий чугун можно использовать для производства тормозов, дисков сцепления, а также деталей для насосов;
- жаростойкий – для доменных, термических, мартеновских печей;
- жаропрочный – для компрессорного оборудования, дизельных двигателей;
- высококачественная сталь используется для газопроводов, корпуса отопительных котлов, сушилок, стиральных и посудомоечных машин.
Заключение
Под железом часто подразумевают не сам метал, а его сплав — низкоуглеродистую электротехническую сталь. Получение чистого железа довольно сложный процесс, и поэтому его используют только для производства магнитных материалов. Как уже отмечалось, что исключительное физическое свойство простого вещества железа – это ферромагнетизм, т. е. способность намагничиваться в присутствии магнитного поля.
Где встречается железо в природе
ХиМуЛя.com

Владельцы сайта
- Галина Пчёлкина

Урок №51. Железо. Положение железа в периодической системе и строение его атома. Нахождение в природе. Физические и химические свойства железа.
Железо – химический элемент
1. Положение железа в периодической таблице химических элементов и строение его атома
Железо — это d- элемент VIII группы; порядковый номер – 26; атомная масса Ar ( Fe ) = 56; состав атома: 26-протонов; 30 – нейтронов; 26 – электронов.
Схема строения атома:

Электронная формула: 1s 2 2s 2 2p 6 3s 2 3p 6 3d 6 4s 2
Металл средней активности, восстановитель:
Fe 0 -2 e — → Fe +2 , окисляется восстановитель
Fe 0 -3 e — → Fe +3 , окисляется восстановитель
Основные степени окисления: +2, +3

2. Распространённость железа
Железо – один из самых распространенных элементов в природе . В земной коре его массовая доля составляет 5,1%, по этому показателю оно уступает только кислороду, кремнию и алюминию. Много железа находится и в небесных телах, что установлено по данным спектрального анализа. В образцах лунного грунта, которые доставила автоматическая станция “Луна”, обнаружено железо в неокисленном состоянии.
Железные руды довольно широко распространены на Земле. Названия гор на Урале говорят сами за себя: Высокая, Магнитная, Железная. Агрохимики в почвах находят соединения железа.
Железо входит в состав большинства горных пород. Для получения железа используют железные руды с содержанием железа 30-70% и более.
Основными железными рудами являются :
магнетит (магнитный железняк) – Fe3O4 содержит 72% железа, месторождения встречаются на Южном Урале, Курской магнитной аномалии:


гематит (железный блеск, кровавик)– Fe2O3 содержит до 65% железа, такие месторождения встречаются в Криворожском районе:


лимонит (бурый железняк) – Fe2O3*nH2O содержит до 60% железа, месторождения встречаются в Крыму:

пирит (серный колчедан, железный колчедан, кошачье золото) – FeS2 содержит примерно 47% железа, месторождения встречаются на Урале.

3. Роль железа в жизни человека и растений
Биохимики открыли важную роль железа в жизни растений, животных и человека. Входя в состав чрезвычайно сложно построенного органического соединения, называемого гемоглобином, железо обусловливает красную окраску этого вещества, от которого в свою очередь, зависит цвет крови человека и животных. В организме взрослого человека содержится 3 г чистого железа, 75% которого входит в состав гемоглобина. Основная роль гемоглобина – перенос кислорода из легких к тканям, а в обратном направлении – CO2.
Железо необходимо и растениям. Оно входит в состав цитоплазмы, участвует в процессе фотосинтеза. Растения, выращенные на субстрате, не содержащем железа, имеют белые листья. Маленькая добавка железа к субстрату – и они приобретают зеленый цвет. Больше того, стоит белый лист смазать раствором соли, содержащей железо, и вскоре смазанное место зеленеет.
Так от одной и той же причины – наличия железа в соках и тканях – весело зеленеют листья растений и ярко румянятся щеки человека.
4. Физические свойства железа.
Железо – это серебристо-белый металл с температурой плавления 1539 о С. Очень пластичный, поэтому легко обрабатывается, куется, прокатывается, штампуется. Железо обладает способностью намагничиваться и размагничиваться, поэтому применяется в качестве сердечников электромагнитов в различных электрических машинах и аппаратах. Ему можно придать большую прочность и твердость методами термического и механического воздействия, например, с помощью закалки и прокатки.
Различают химически чистое и технически чистое железо. Технически чистое железо, по сути, представляет собой низкоуглеродистую сталь, оно содержит 0,02 -0,04% углерода, а кислорода, серы, азота и фосфора – еще меньше. Химически чистое железо содержит менее 0,01% примесей. Химически чистое железо – серебристо-серый, блестящий, по внешнему виду очень похожий на платину металл. Химически чистое железо устойчиво к коррозии и хорошо сопротивляется действию кислот. Однако ничтожные доли примесей лишают его этих драгоценный свойств.
Восстановлением из оксидов углём или оксидом углерода (II), а также водородом:
6. Химические свойства железа
Как элемент побочной подгруппы железо может проявлять несколько степеней окисления. Мы рассмотрим только соединения, в которых железо проявляет степени окисления +2 и +3. Таким образом, можно говорить, что у железа имеется два ряда соединений, в которых оно двух- и трехвалентно.
1) На воздухе железо легко окисляется в присутствии влаги (ржавление):
2) Накалённая железная проволока горит в кислороде, образуя окалину — оксид железа (II,III) — вещество чёрного цвета:
3) При высокой температуре (700–900°C) железо реагирует с парами воды:
4) Железо реагирует с неметаллами при нагревании:
5) Железо легко растворяется в соляной и разбавленной серной кислотах при обычных условиях:
6) В концентрированных кислотах – окислителях железо растворяется только при нагревании
На холоде концентрированные азотная и серная кислоты пассивируют железо!
7) Железо вытесняет металлы, стоящие правее его в ряду напряжений из растворов их солей.
8) Качественные реакции на
Основная часть получаемого в мире железа используется для получения чугуна и стали — сплавов железа с углеродом и другими металлами. Чугуны содержат около 4% углерода. Стали содержат углерода менее 1,4%.
Чугуны необходимы для производства различных отливок — станин тяжелых машин и т.п.
Стали используются для изготовления машин, различных строительных материалов, балок, листов, проката, рельсов, инструмента и множества других изделий. Для производства различных сортов сталей применяют так называемые легирующие добавки, которыми служат различные металлы: М n , С r , Мо и другие, улучшающие качество стали.
Задания для закрепления
№1. Составьте уравнения реакций получения железа из его оксидов Fe2O3 и Fe3O4 , используя в качестве восстановителя:
а) водород;
б) алюминий;
в) оксид углерода (II).
Для каждой реакции составьте электронный баланс.
№2. Осуществите превращения по схеме:
Fe2O3 -> Fe — +H2O, t -> X — +CO, t -> Y — +HCl -> Z
Назовите продукты X, Y, Z?
Глоссарий. Химия
Желе́зо — элемент побочной подгруппы восьмой группы четвёртого периода периодической системы химических элементов с атомным номером 26. Обозначается символом Fe (лат. Ferrum). Один из самых распространённых в земной коре металлов (второе место после алюминия). Простое вещество железо (CAS-номер: 7439-89-6) — ковкий металл серебристо-белого цвета с высокой химической реакционной способностью: железо быстро корродирует при высоких температурах или при высокой влажности на воздухе. В чистом кислороде железо горит, а в мелкодисперсном состоянии самовозгорается и на воздухе. На самом деле железом обычно называют его сплавы с малым содержанием примесей (до 0,8 %), которые сохраняют мягкость и пластичность чистого металла. Но на практике чаще применяются сплавы железа с углеродом: сталь (до 2,14 вес. % углерода) и чугун (более 2,14 вес. % углерода), а также нержавеющая (легированная) сталь с добавками легирующих металлов (хром, марганец, никель и др.). Совокупность специфических свойств железа и его сплавов делают его «металлом № 1» по важности для человека. В природе железо редко встречается в чистом виде, чаще всего оно встречается в составе железо-никелевых метеоритов. Распространённость железа в земной коре — 4,65 % (4-е место после O, Si, Al). Считается также, что железо составляет бо́льшую часть земного ядра.
Происхождение названия
Имеется несколько версий происхождения славянского слова «железо» (белор. жалеза, укр. залізо, ст.-слав. желѣзо, болг. желязо, сербохорв. жељезо, польск. żelazo, чеш. železo, словен. železo). Одна из этимологий связывает праслав. *želězo с греческим словом χαλκός, что означало железо и медь, согласно другой версии *želězo родственно словам *žely «черепаха» и *glazъ «скала», с общей семой «камень». Третья версия предполагает древнее заимствование из неизвестного языка. Романские языки (итал. ferro, фр. fer, исп. hierro, порт. ferro, рум. fier) продолжают лат. ferrum . Латинское ferrum ( Германские языки заимствовали название железа (готск. eisarn,англ. iron, нем. Eisen, нидерл. ijzer,дат. jern, швед. järn) из кельтских. Пракельтское слово *isarno- (> др.-ирл. iarn, др.-брет. hoiarn), вероятно, восходит к пра-и.е. *h1esh2r-no- «кровавый» с семантическим развитием «кровавый» > «красный» > «железо». Согласно другой гипотезе данное слово восходит к пра-и.е. *(H)ish2ro- «сильный, святой, обладающий сверхъестественной силой». Древнегреческое слово σίδηρος, возможно, было заимствовано из того же источника, что и славянское, германское и балтийское слова для серебра. Название природного карбоната железа (сидерита) происходит от лат. sidereus — звёздный; действительно, первое железо, попавшее в руки людям, было метеоритного происхождения. Возможно, это совпадение не случайно. В частности древнегреческое слово сидерос (σίδηρος) для железа и латинское sidus, означающее «звезда», вероятно, имеют общее происхождение.
Получение
В промышленности железо получают из железной руды, в основном из гематита (Fe2O3) и магнетита (FeO·Fe2O3). Существуют различные способы извлечения железа из руд. Наиболее распространённым является доменный процесс. Первый этап производства — восстановление железа углеродом в доменной печи при температуре 2000 °C. В доменной печи углерод в виде кокса, железная руда в виде агломерата или окатышей и флюс (например, известняк) подаются сверху, а снизу их встречает поток нагнетаемого горячего воздуха. В печи углерод в виде кокса окисляется до монооксида углерода. Данный оксид образуется при горении в недостатке кислорода. В свою очередь, монооксид углерода восстанавливает железо из руды. Чтобы данная реакция шла быстрее, нагретый угарный газ пропускают через оксид железа(III). Флюс добавляется для избавления от нежелательных примесей (в первую очередь от силикатов; например кварц) в добываемой руде. Типичный флюс содержит известняк (карбонат кальция) и доломит (карбонат магния). Для устранения других примесей используют другие флюсы. Действие флюса (в данном случае карбонат кальция) заключается в том, что при его нагревании он разлагается до его оксида. Оксид кальция соединяется с диоксидом кремния, образуя шлак — метасиликат кальция. Шлак, в отличие от диоксида кремния, плавится в печи. Более лёгкий, чем железо, шлак плавает на поверхности — это свойство позволяет разделять шлак от металла. Шлак затем может использоваться при строительстве и сельском хозяйстве. Расплав железа, полученный в доменной печи, содержит довольно много углерода (чугун). Кроме таких случаев, когда чугун используется непосредственно, он требует дальнейшей переработки. Излишки углерода и другие примеси (сера, фосфор) удаляют из чугуна окислением в мартеновских печах или в конвертерах. Электрические печи используются и для выплавки легированных сталей. Кроме доменного процесса, распространён процесс прямого получения железа. В этом случае предварительно измельчённую руду смешивают с особой глиной, формируя окатыши. Окатыши обжигают, и обрабатывают в шахтной печи горячими продуктами конверсии метана, которые содержат водород. Водород легко восстанавливает железо, при этом не происходит загрязнения железа такими примесями как сера и фосфор, которые являются обычными примесями в каменном угле. Железо получается в твёрдом виде, и в дальнейшем переплавляется в электрических печах. Химически чистое железо получается электролизом растворов его солей.

