Электролит для золочения своими руками
Золочение в домашних условиях
При применении технологии золочения можно вернуть былую привлекательность практически любому украшению из меди или серебра. Изделия с позолотой применяются самым различным образом, чаще всего они становятся украшением. Золочение в домашних условиях может проводится при применении самых различных технологий. Покрыть золотом можно изделия из серебра или других сплавов, главное знать все особенности процесса. Восстановление позолоты лучше всего провести в домашних условиях при применении специальных веществ и оборудования.

Различные методики нанесения позолоты
Качество получаемой поверхности во многом зависит от особенностей применяемой технологии. Наибольшее распространение получили следующие:
- Гальванический метод покрытие позолотой.
- Применение специальных химических веществ.
- Механический способ нанесения требуемого вещества.
В каждом случае применяются определенные инструменты и химические реактивы.
При этом некоторые технологии подходят для покрытия цепочек в домашних условиях, другие обработки иных изделий по предназначению.
Химический способ
Химическое золочение серебра или другого сплава представляет собой процесс нанесения хлорида золота на обрабатываемую поверхность. Рекомендации по созданию требуемого реагента следующие:
- Металл нужно расковать на заранее подготовленную фольгу. Все элементы должны быть измельчены до небольших элементов.
- Небольшие кусочки погружаются в смесь подготовленного заранее химического реагента. Раствор создается при сочетании 30 грамм концентрата соляной и 10 грамм азотной кислоты. Стоит учитывать, что с подобными веществами в домашних условиях нужно работать аккуратно.
- На один грамм напыления приходится не менее 10 мл раствора. Именно поэтому следует заранее рассчитать требуемое количество жидкости.

Раствор для золочения
Для смешивания активных реагентов используется фарфоровая посуда. Процесс растворения может длиться в течение трех суток. После предварительной подготовки металла его выпаривают при температуре около 80 °C до появления жидкости. На момент выпаривания следует время от времени помешивать получаемую консистенцию стеклянной палочкой, за счет чего получится однородный состав.
Проводя золочение металла нужно качественно подготовить требуемый состав. Для этого потребуется:
- Вода, очищенная от примесей, при температуре 60 °C.
- Около 15 грамм сиропа хлорной соли золота.
- Более 65 грамм карбоната калия или хлорида натрия. Оба вещества должный пройти качественную очистку.
Покрывать поверхность серебряных или иных изделий следует только после его подготовки. Для этого проводится обезжиривание при применении 20% едким натрием, после чего изделие промывается в 25% растворе соды.

После подготовки поверхности изделие покрывается в ранее подготовленную смесь. Через некоторое время оно становится позолоченным. После извлечения и высыхания поверхности ее промывают и вытирают сухой тканью. Для придания более привлекательного вида позолота полируется шерстяной тканью.
Механические способы золочения
Золотое напыление характеризуется определенными качествами, которые делают изделие более привлекательным и устойчивым к воздействию окружающей среды. Механическое нанесение позолоты проводится крайне редко, так как добиться однородности поверхностного слоя достаточно сложно. К особенностям рассматриваемой технологии можно отнести нижеприведенные моменты:
- При подобном золочении применяется специальная паста. Ее можно приготовить в специализированном магазине или изготовить своими руками. Состав пасты может существенно отличаться, что стоит учитывать.
- Слой, получаемый при применении механического способа золочения в домашних условиях, имеет небольшую толщину. Именно поэтому получаемое покрытие не прослужит на протяжении длительного периода.
- В состав распространенных веществ входит желтая кровяная соль, порошок из мела и винный камень.
- Рекомендуется смешивать пасту с водой для получения однородной кашицы, которое втирается в поверхность при помощи шерстяной ткани.
- Перед золочением в домашних условиях поверхность должна быть обезжирена. Для этого также применяются специальные составы.
- Нанести пасту позолоты следует равномерным слоем, при втирании уделяется внимание тому, чтобы вещество не попадало на отрытые участки кожи.

Нанесение позолоты вручную
Механическая технология достаточно сложна в исполнении. Как правило, она применяется в том случае, если нужно покрыть в домашних условиях только часть изделия. Это связано с тем, что другие технологии покрытия предусматривают полное окунание изделия в специальный раствор.
Золочение методом гальваники
Толстый слой позолоты высокого качества можно получить при применении особой технологии. Она предусматривает погружение заготовки в специальный электролит. Гальваническим методом проводится обработка самых различных заготовок, так как он напоминает распространенные электрохимические процессы.
Стоит учитывать, что в зависимости от типа применяемого раствора поверхность может приобретать самые различные оттенки. Электролит для золочения своими руками в домашних условиях можно изготовить следующим образом:
- На 700 мл очищенной воды добавляется 60 грамм фосфорнокислого натрия.
- При использовании 2,5 грамма хлорного золота для их растворения используется 150 мл воды.
- В 150 мл дистиллированной воды растворяют 10 грамм сернистокислого натрия, а также один грамм цианистого калия.
С подобными реагентами следует работать аккуратно. Гальваника золотом в домашних условиях проводится при нагреве раствора до температуры около 60 °C, для активации химического процесса для истощения электролита устанавливается анод.
На обработку заготовок в подобном растворе уходит около 15 часов. Существенно повысить эффективность процесса помогает ток малой силы. За счет этого на поверхности образуется матовая пленка из золота.
Приготовление раствора для золочения
Раствор для золочения в домашних условиях должен приготавливаться с особой осторожностью. Это связано с тем, что при контакте веществ образуется химическая реакция, которая может привести к появлению вредных выделений. Для создания требуемого состава могут смешиваться следующие компоненты:
- Хлорное золото.
- Поваренная соль.
- Цианистый калий.
- Сода и дистиллированная вода.
Подобный состав больше всего подходит для обработки обычного металла. Покрытие золотом в домашних условиях серебряной поверхностью может проводится при создании следующего состава:
- Хлорное золото.
- Карбонат калия.
- Пищевая соль.
- Железистосинеродистый калий.
Все элементы смешиваются в воде до получения однородной консистенции. Работать следует исключительно в защитной экипировке, попадание вещества на открытые участки тела или в дыхательные пути не допускается.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Золочение металлов своими руками

В данной статье будет рассмотрено несколько способов золочения металлов своими руками:
Натиранием хлорным золотом
Растворяют золото в царской водке, осторожно выпаривают жидкость досуха, растворяют остаток, состоящий из хлорного золота, в растворе цианистого калия и прибавляют столько отмученного мела, чтобы получилась жидкая кашица. При помощи кисти покрывают этой кашицей металлический предмет. Через некоторое время его обмывают и полируют позолоченный слой.
Для золочения железа и стали можно пользоваться раствором хлорного золота в эфире. Раствор наносится на металлическую поверхность. После испарения эфира поверхность натирают чистой тряпкой.
Если по железу или стали рисовать гусиным пером, смоченным в указанном выше растворе, то можно получить золотой узор. Для золочения цинка приготовляется паста, состоящая из 20 гр хлорного золота, 60 гр цианистого калия в 100 мл воды. Взбалтывают, фильтруют и к фильтрату прибавляют смесь из 5 гр винного камня и 100 гр мела. Смесь мела и винного камня прибавляют, пока не образуется каша, которая и наносится на предмет при помощи кисти или щетки.
Для золочения серебра применяют один из следующих растворов:
Жидкость для золочения:
Растворяют золото в смеси соляной и азотной кислот, разбавленных водой. К раствору прибавляют поташ и выливают этот раствор в железный котел с 2 л кипящей воды. Жидкость кипятят в течение 2 часов.
Предметы, подлежащие золочению, прокаливают, затем травят сначала раствором серной кислоты, а потом, на мгновение, азотной кислотой. Связывают латунной проволокой, быстро опускают в смесь из серной, азотной и соляной кислот, тотчас же вынимают. Ополаскивают водой, погружают в ртуть, а затем в воду, а через 30 секунд — в ванну с жидкостью для золочения. Промывают и сушат в горячих древесных опилках. Если слой золота должен быть немного толще, к предметам во время пребывания их в ванне прикасаются цинком.
Для окрашивания позолоченных предметов применяют следующий раствор:
- сернокальциевой соли 10 гр.
Прибавляют небольшое количество воды, нагревают до кипения, опускают в раствор предметы, затем сушат их на открытом огне, пока они не покроются коричневой пленкой, смывают эту пленку и тем заканчивают окрашивание.
Погружение с цинковым контактом
Очищенные от грязи и жира металлические предметы опускают в нагретый раствор. Контактом служит цинковая палочка.
Для золочения меди и латуни применяют следующий состав:
В 1.5 л воды растворяют фосфорнонатриевую соль и едкий кали. Отдельно в 0.5 л воды растворяют цианистый калий и хлорное золото, и оба раствора смешивают. Раствор при употреблении нагревают до кипения.
При золочении железа, стали, цинка и олова необходимо предварительно покрыть их слоем меди.
Этот состав может работать почти до полного израсходования в нем золота и не разлагается при хранение Если состав перестанет действовать, прибавляют немного (около 10 гр) цианистого калия.
Существует множество различных способов кодирования от алкоголизма. Вы можете узнать подробнее о них. Будет интересно.
Золочение гальваническим путем
Наиболее прочной окраской золотых сплавов является золочение гальваническим путем в соответствующих составных золотых ваннах, чем достигается красноватое или светло-желтое золочение, смотря по тому, содержат ли ванны в себе медь или серебро.
Растворяют 60 гр фосфорнокислого натрия в 700 мл воды, отдельно растворяют 2,5 гр хлорного золота в 150 мл воды и, наконец, 1 гр цианистого калия и 10 гр двусернистокислого натрия в 150 мл воды. Сперва соединяют два первых раствора понемногу между собой, а потом примешивают третий раствор. Эту жидкость употребляют при 50—62°, пользуются платиновым анодом и прибавляют хлорного золота, когда раствор истощен.
Золотая ванна по Зельми для гальванического золочения серебра, олова, железа, меди, латуни, альфенида без предшествующей подкладки. 1 гр кристаллич. углекислого натрия и 1 гр желтой кровяной соли нагревают в фарфоровой чашке до кипения с 30 гр воды, прибавляют осажденное гремучее золото (полученное из 50 гр хлорного золота осаждением с нашатырным спиртом) кипятят в течение 12 мин., пока не образуется пушистый красный осадок и жидкость не примет красивого золотистого цвета, снимают с огня и фильтруют сквозь тонкую фильтровальную бумагу.
Во время кипения нужно заменять испаряющуюся воду, т. е. добавить ее столько, чтобы фильтрат весил 65 гр. Эту золотую ванну применяют со слабым током при помощи элемента Даниеля и после 15-16 часов получается красивая матовая позолота.
Если хотят железную проволоку покрыть матовой позолотой, то ее предварительно кладут для протравы в разбавленную серную кислоту (10 на 100 воды); затем протягивают через крепкую азотную кислоту, к которой прибавлено немного голландской сажи, и, наконец, помещают проволоку в медный раствор, состоящий из 1,6 кг едкого натрия, 1,5 гр винного камня, 350 гр медного купороса, 10 л воды, и соединяют ее жестяными или цинковыми полосами.
Покрытая таким образом медью железная проволока готова для позолоты. Растворяют, с одной стороны, 150 гр цианистого калия в 5 л воды и прибавляют 10 гр хлорного золота; с другой стороны,растворяют 50 гр фосфорнокислого натра в 5 л воды и прибавляют 50 гр едкого калия. Оба раствора смешивают нагреванием до кипения и кладут туда железную проволоку, которую через короткое время можно вынуть позолоченной.
Покрытие золотом в домашних условиях: методы золочения
Научившись выполнять золочение в домашних условиях, что не так сложно, как может показаться на первый взгляд, вы сможете вернуть вторую жизнь любимым украшениям из меди и серебра. Изделия, изготовленные из золота, уже на протяжении многих лет пользуются огромной популярностью как у женщин, так и у мужчин. Чтобы обладать такими изделиями без серьезных затрат на их приобретение, достаточно овладеть технологией золочения.

Покрыть позолотой можно как цветные сплавы, так и сталь или чугун
На изделия из каких металлов можно наносить слой позолоты
Наиболее распространенным процессом является золочение серебра, но золотое покрытие можно наносить и на поверхность других металлов. Так, позолота может быть нанесена на изделия из меди, латуни и цинка, а также из железа и стали и др.
На вопрос о том, как позолотить металл в домашних условиях, однозначного ответа не существует. Все зависит от того, изделия из какого металла необходимо подвергнуть такой обработке. На выбор технологии золочения, осуществляемого в домашних условиях, влияет также результат, которого необходимо добиться.

С помощью золочения можно придать обычным вещам совершенно другой вид
Для золочения металла могут использоваться разные методы, наиболее распространенными из которых являются:
- натирание поверхности изделия раствором хлорного золота;
- золочение, выполняемое погружением изделия в раствор с цинковым контактом;
- гальваническое золочение.
Каждый из таких методов золочения, выполняемого в домашних условиях, требует использования определенных химических реактивов, инструментов и оборудования.
Приготовление и использование хлорного золота
Чтобы покрыть слоем позолоты металл, часто используют раствор, называемый хлорным золотом. Для приготовления такого раствора золото растворяют в «царской водке», представляющей собой смесь соляной и азотной кислот. Соляную и азотную кислоты берут в пропорции 3 : 1. Золото помещают в этот состав, а затем выпаривают жидкость. Выполнять процедуру выпаривания жидкости из такого раствора следует очень аккуратно, чтобы не получить ожоги кожных покровов и дыхательных путей. Сухое вещество, оставшееся после выпаривания, как раз и является хлорным золотом.

При выпаривании нужно отделить открытый огонь от емкости с раствором, например, сделав прослойку из асбестовой крошки, насыпанной в отдельную посудину
Перед тем как применять хлорное золото для позолоты, его необходимо смешать с раствором цианистого калия и отмученным мелом, в результате чего должна получиться кашицеобразная масса. Такой кашицей, используя кисточку, покрывают изделие, после чего его выдерживают некоторое время, а затем тщательно промывают и полируют.
Для золочения стали хлорное золото смешивают с эфиром. Покрытое таким составом изделие оставляют на некоторое время, пока эфир полностью не испарится, а затем обработанную поверхность просто натирают тканью для придания золотого блеска.
Используя хлорное золото, предварительно смешанное с эфиром, на металлический предмет можно наносить различные надписи и узоры. Для того чтобы провести такую процедуру, в полученный раствор окунают гусиное перо и выполняют требуемые надписи и узоры, которые после испарения эфира и полировки будут сверкать золотым блеском.

Большие поверхности покрывают позолотой с помощью мягкой кисти
Как уже говорилось выше, золотое напыление часто наносят на серебро, для чего также может использоваться хлорное золото. Чтобы выполнить химическое золочение изделий из данного металла, необходимо приготовить смесь, включающую в себя следующие компоненты:
- хлорное золото – 10 граммов;
- цианистый калий – 30 граммов;
- поваренную соль – 20 граммов;
- соду – 20 граммов;
- воду – 1,5 л.
Химическое золочение, которому необходимо подвергнуть серебро, можно также выполнять с использованием смеси из:
- хлорного золота – 7 граммов;
- железистосинеродистого калия – 30 граммов;
- карбоната калия – 30 граммов;
- пищевой соли – 30 граммов;
- воды – 1 л.
Саму процедуру напыления слоя золота на поверхность металла при использовании химических растворов выполняют в следующей последовательности.
- Обрабатываемое изделие предварительно прокаливают.
- Поверхность предмета протравливают сначала раствором серной кислоты, а затем азотной кислотой.
- Протравленное изделие на мгновение опускают в смесь, состоящую из серной, азотной и соляной кислот.
- После обработки в смеси кислот изделие ополаскивают водой, затем погружают в ртуть и наконец в воду, где его выдерживают 30 секунд.
- После емкости с водой изделие помещают в раствор для золочения, выдерживают требуемое время, затем промывают водой и сушат в древесных опилках.
Применение цинкового контакта
Чтобы получить более толстый позолоченный слой, используют цинковый контакт. Таким методом можно, например, покрыть слоем золота серебро. Для золочения готовят состав из таких компонентов, как:
- хлорное золото – 15 граммов;
- углекалиевая соль – 65 граммов;
- желтая кровяная соль – 65 граммов;
- пищевая соль – 65 граммов;
- вода – 2 л.

Потребуется некоторое время на растворение всех компонентов состава
Изделия, изготовленные из меди и латуни, покрываются под золото в растворе следующего состава:
- хлорное золото – 2 грамма;
- едкий калий – 6 граммов;
- цианистый калий – 32 грамма;
- фосфорнонатриевая соль – 10 граммов;
- вода – 2 л.
Предметы, на поверхность которых необходимо нанести слой позолоты, тщательно очищаются от грязи и жира, затем их помещают в предварительно нагретый состав для золочения. Уже находящиеся там изделия соединяют с цинковой палочкой, которая и выступает в качестве контакта.
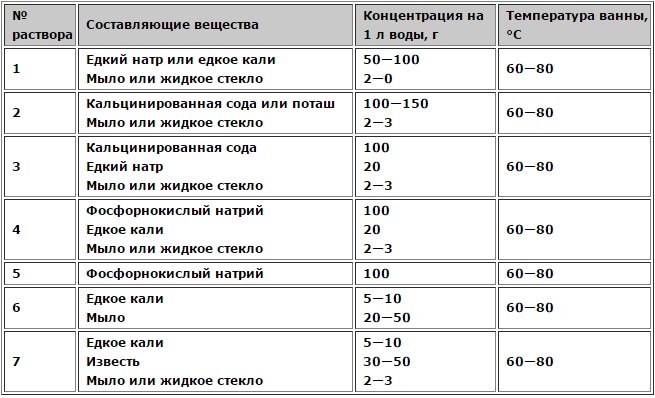
Составы обезжиривающих растворов
Чтобы позолота, нанесенная на поверхность изделий из стали, цинка и олова, была качественной и отличалась хорошей адгезией, перед золочением их необходимо подвергнуть процедуре омеднения.
Гальванический метод нанесения позолоты
Наиболее прочный и качественный слой позолоты позволяет получить гальваническое покрытие золотом, выполняемое в специальных электролитических растворах. Такая технология золочения очень напоминает цинкование, так как для ее реализации используются гальваника и аналогичные электрохимические процессы.
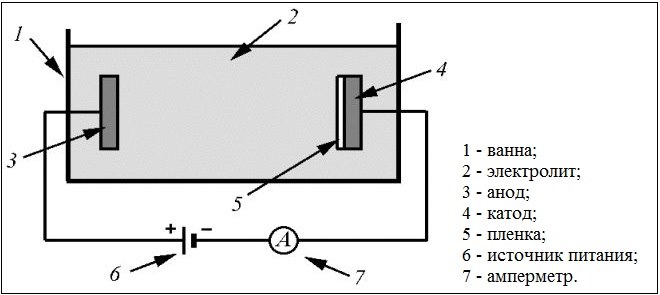
Схема гальванической ванны
В зависимости от химического состава раствора, в котором выполняется гальванизация, сформированная позолота может иметь красноватый или светло-желтый оттенок. В основном золочение изделий из металла по данной технологии выполняют в растворах двух типов.
Электролиты для золочения первого типа готовят в следующей последовательности.
- В 700 миллилитрах воды растворяют 60 граммов фосфорнокислого натрия.
- В 150 миллилитрах воды разводят 2,5 грамма хлорного золота.
- В других 150 миллилитрах воды растворяют 1 грамм цианистого калия и 10 граммов двусернистокислого натрия.
- Сначала аккуратно смешивают два первых раствора, а затем в полученную смесь добавляют третий.
Чтобы позолотить серебро или любой другой металл таким методом, приготовленный состав доводят до температуры 50–62° и используют для протекания процесса платиновый анод. После истощения такого электролита для золочения в него добавляют хлорное золото.
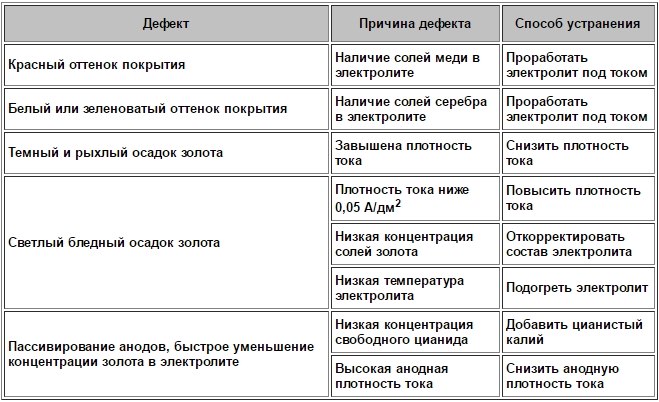
Дефекты при использовании электролитов золочения и способы их устранения
Второй тип электролита для золочения носит название «золотая ванна Зельми». В таком растворе золотят серебро, сталь, изделия из олова, меди, латуни, христофлевого металла. Приготовление этого электролита для золочения происходит в несколько этапов.
- В фарфоровой емкости доводят до кипения 30 миллилитров воды, смешанные с кристаллическим углекислым натрием и железистосинеродистым калием (взятых по 1 грамму).
- В полученный раствор добавляют осажденное аммиаком гремучее золото и кипятят в течение двенадцати минут.
- После образования красного пушистого осадка полученную жидкость, которая должна иметь насыщенный золотистый цвет, фильтруют.
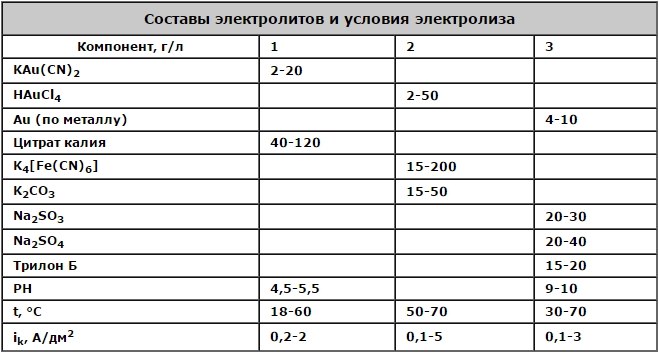
Менее токсичными считаются условно бесцианидные электролиты золочения, характеристики которых приведены в таблице
Обработку в таком электролите для золочения проводят на протяжении 15–16 часов, используя для этого элемент Даниэля и слабые токи. В результате на поверхности металлического изделия формируется эффектная матовая позолота.
Задаваясь вопросами о том, что такое золочение и как его выполнить, следует учитывать, что для его осуществления используются различные методики, только часть из которых описана выше. Выбирая из таких технологий оптимальную, надо принимать во внимание целый ряд факторов, а также ориентироваться на желаемый результат.
Различные способы нанесения позолоты в домашних условиях
Золочение в домашних условиях осуществляют двумя способами: электролитическим (гальваническим) и химическим. Для покрытия изделий позолотой требуются реактивы, которых не найти в свободной продаже: цианид калия, азотная и соляная кислоты. Также необходимо специальное оборудование: электролитические ванны и источник постоянного тока. Процесс золочения достаточно трудоемкий, требует сноровки, аккуратности и некоторого опыта.
Химический способ
А) Химическое золочение — процесс нанесения хлорида золота на металл, из которого сделано изделие. Хлорное золото готовится так: металл нужно расковать в фольгу и измельчить на мелкие кусочки, погрузить их в смесь азотной и соляной кислот (в так называемую царскую водку). Необходимо взять 30 г концентрированной соляной и 10 г концентрированной азотной кислот. На 1 г золота должно приходиться 10 мл раствора.

Нанесение позолоты в домашних условиях
Растворение должно происходить в фарфоровой посуде, процесс может длиться от нескольких часов до 2-3 суток. Когда металл полностью растворится, необходимо выпарить смесь в водяной бане при 70-80 градусах до появления вязкой золотистой жидкости. При выпаривании раствор помешивают стеклянной палочкой.
Чтобы приготовить смесь для золочения, потребуются:
- Горячая очищенная (дистиллированная) вода (50-60 градусов) в объеме 2 литра.
- 15 г сиропа хлорной соли золота.
- По 65 г карбоната калия (поташа) и хлорида натрия высокой очистки (соль «Экстра»).
Перед нанесением позолоты поверхность предмета необходимо обезжирить 10-20% едким натрием или кипячением в растворе соды. Далее промывают изделие в 25% растворе соляной кислоты, т. е. протравливают. После обезжиривания необходимо промыть предмет в воде.
Далее погружают изделие для позолочения в приготовленную смесь из горячей воды, поташа, хлорида натрия и хлорного золота. Предмета касаются цинковой палочкой, через некоторое время он становится позолоченным. После этого его извлекают и промывают, вытирают насухо и полируют при помощи шерстяной ткани.
Б) Помимо метода химического золочения используют метод натирания при помощи пасты. При таком способе нанесения позолоты слой покрытия тоньше. В состав пасты для натирания входит желтая кровяная соль (гексацианоферрат [II] калия), винный камень, порошок из мела, хлорное золото. Для изготовления 100 г пасты берут 55 г мела, 5 г кремортартара, 30 г желтого гексацианоферрата калия и 10 г хлорида золота, ингредиенты перемешивают. Полученную пасту разбавляют водой до образования кашицы. Этой смесью натирают обезжиренное изделие при помощи шерстяной ткани.
В) Существует третий метод покрытия. Для этого 10 г золота растворяют в смеси азотной и соляной кислоты, воды — всех компонентов взять по 25 г. Добавляют в этот состав 300 г поташа (карбоната калия). Готовят котел, в котором кипятится вода (2 л), вливают в нее эту смесь. Кипячение продолжается 2 часа.
Украшения, нуждающиеся в позолочении, прокаливают и протравливают сначала серной кислотой, потом азотной. Затем изделие обматывают проволокой из латуни (сплав цинка и меди), и погружают на мгновение в смесь азотной, серной и соляной кислот. Потом предметы ополаскивают, далее поочередно загружают их в ртуть, а потом в воду. Через полминуты их окунают в приготовленную жидкость, моют, высушивают в горячих опилках.

Изделие с позолотой
1) Железо и сталь.
Чтобы покрыть позолотой изделия из стали и железа, необходимо растворить сироп хлорида золота в эфире. Полученным составом, нанесенным на тряпочку, покрывают и натирают поверхность предмета из стали или железа. Затем эфир испаряется, а золото остается.
Если необходимо не просто покрыть позолотой изделие, а сделать на нем узор, то в смеси эфира с хлорным золотом смачивают перо и проводят им по предмету.
Желательно до позолочения предметов из железа, стали, олова, цинка покрывать поверхность медью, так как на нее лучше ложится позолота.
2) Цинковые предметы.
Покрытие цинковых изделий осуществляется при помощи натирания их пастой. Готовится она из 60 г цианида калия, 20 г хлорного золота и 100 г воды — эти ингредиенты смешиваются. В данный раствор добавляют 5 г кремортартрата и 100 г порошка карбоната кальция (мела). Полученный состав наносят при помощи щеточки или кисти.
Для покрытия серебряных украшений есть два варианта раствора, в которые погружают предметы:
- 10 г хлорида золота, 30 г калия цианида, соды и хлорида натрия по 20 г, полтора литра воды.
- 7 г хлорида золота, по 30 г поташа, желтого гексацианоферрата калия и хлорида натрия, литр воды.
Во время погружения изделия необходимо прикоснуться к нему цинковой палочкой и оно начнет покрываться золотом. После этого предмет извлекается из раствора, промывается и вытирается, полируется шерстяной тряпкой.
Хлорид золота (2 г) и цианид калия (32 г) растворяют в 0,5 л воды. В других полутора литрах воды тем временем растворяют едкий калий (6 г) и фосфорно-натриевую соль (10 г). Смешивают оба раствора и кипятят.
Гальваника
Существует два способа:
- Готовят три раствора: 60 г фосфата натрия с 700 г воды; 2,5 г хлорида золота и 150 г воды; 1 г цианида калия и 10 г сульфата натрия со 150 г воды. Первые два раствора смешивают, третий добавляют последним. Температура — 50-60 градусов. Анод — из платины. При истощении электролитного раствора добавляют хлорид золота.
- Ванна по Зельми: по 1 г гексацианоферрата калия (желтого) и карбоната натрия смешать с 30 г воды, нагреть в чашке из фарфора. Добавить в смесь осажденное нашатырным спиртом золото. Кипятить в течение 10-12 минут. При испарении воды ее добавляют, пропускают через раствор ток элемента Даниеля. Время воздействия — 15-16 часов.
Способы позолоты в домашних условиях трудоемки и не всегда доступны. Предпочтителен метод химического золочения или натирания.
Золочение
Золотые покрытия можно наносить непосредственно на медь, медные сплавы, серебро и никель. Наилучшие результаты при золочении металлов обеспечивает нанесение золота на никель. Введение в состав золотых осадков кобальта, меди, серебра, сурьмы, индия и некоторых других металлов, дает возможность получать золотые сплавы различных цветов, и имеющих улучшенные эксплуатационные свойства.  Такие сплавы характеризуются мелкокристаллической структурой, низкой пористостью, повышенным блеском и высокой износостойкостью. Золотосеребряные сплавы — “зеленое” золото или золотомедные — “розовое” золото наносят только на подслой золота, серебра или сплавов золота. Из электролита “розовое” золото можно осаждать золотомедные сплавы значительной толщины и обладающие наибольшей твердостью среди всех двойных сплавов на основе золота. К тому же цвет получаемых покрытий при массовой доле золота в сплаве, равной 85%, почти не отличим от цвета металлургического золота 585-й пробы.
Такие сплавы характеризуются мелкокристаллической структурой, низкой пористостью, повышенным блеском и высокой износостойкостью. Золотосеребряные сплавы — “зеленое” золото или золотомедные — “розовое” золото наносят только на подслой золота, серебра или сплавов золота. Из электролита “розовое” золото можно осаждать золотомедные сплавы значительной толщины и обладающие наибольшей твердостью среди всех двойных сплавов на основе золота. К тому же цвет получаемых покрытий при массовой доле золота в сплаве, равной 85%, почти не отличим от цвета металлургического золота 585-й пробы.
Для нанесения золотых покрытий методом гальванического золочения в основном используются цианистые электролиты золочения, которые большинству показателям обеспечивают наилучшие результаты, по сравнению с не цианистыми электролитами. Основным компонентом в таких электролитах является анион золота, исключающий возможность контактного вытеснения золота медью и другими металлами, а осаждение золота на поверхности детали происходит в результате восстановления металла из цианауратного комплекса. Цианистые электролиты золочения можно разделить на три основные группы: щелочные, нейтральные и кислые.
Щелочные электролиты содержат золото, в пределах 8-12 г/л, свободный цианистый калий или натрий 20-80 г/л, и соль щелочного металла, для повышения электропроводности раствора, 70-100 г/л. Процесс золочения и осаждения золота в щелочных электролитах проводят при катодной плотности тока в диапазоне 0,1–1,1 А/дм 2 , температуре электролита 60-80 о С и постоянном перемешивании. Режимы осаждения в щелочных электролитах несколько ограничены по сравнению с кислыми и нейтральными электролитами золочения, и помимо этого, их основным недостатком является накопление в растворе карбонатов, которые нужно периодически удалять. Щелочные электролиты золочения применяют в основном для получения первичного подслоя золота перед осаждением более толстых золотых покрытий.
Нейтральные электролиты золочения работают при рН = 6,0 — 8,0 и имеют низкое содержание свободного цианида, в пределах 1-2 г/л. Данные электролиты обладают низкой рассеивающей способностью, но имеют более высокий выход по току, чем щелочные электролиты и позволяют получать более низко пористые золотые покрытия. Но использование нейтральных электролитов золочения очень ограничено, так как в процессе работы в них накапливаются соли неблагородных металлов, что отрицательно сказывается на качестве получаемых золотых покрытий. Нейтральные электролиты золочения используются в основном для покрытия сплавами золото-медь и для нанесения покрытий большой толщины 20 мкм и более. Основными недостатками нейтральных электролитов золочения является их нестабильность и необходимость частой регенерации.
 Кислые электролиты золочения работают при рН = 3 – 6, не содержат свободных цианидов, отличаются безвредностью и стабильностью, и имеют самое большое распространение, позволяя проводить процесс золочения при комнатной температуре 20-25 о С и достаточно больших плотностях тока, до 1,5 А/дм 2 , что является их основным преимуществом. И, несмотря на то, что данные электролиты имеют более низкий выход по току, чем щелочные и нейтральные электролиты золочения, они позволяют получать более высоко блестящие золотые покрытия.
Кислые электролиты золочения работают при рН = 3 – 6, не содержат свободных цианидов, отличаются безвредностью и стабильностью, и имеют самое большое распространение, позволяя проводить процесс золочения при комнатной температуре 20-25 о С и достаточно больших плотностях тока, до 1,5 А/дм 2 , что является их основным преимуществом. И, несмотря на то, что данные электролиты имеют более низкий выход по току, чем щелочные и нейтральные электролиты золочения, они позволяют получать более высоко блестящие золотые покрытия.
Комментарий. Перемешивание электролита и повышение концентрации золота в электролите позволяет значительно повысить выход по току, однако увеличение содержания золота в электролите способствует повышению потерь драгоценного металла, поэтому максимальная концентрация его в электролитах не превышает 15 г/л.
Помимо этого, кислые электролиты золочения не содержат свободных цианидов и работают, также как и нейтральные электролиты, с нерастворимыми анодами (в качестве анода используется титановая пластина или сетка с иридиевым или платиновым покрытием).  К недостаткам кислых электролитов золочения можно отнести их относительно низкую рассеивающую способность и более высокие внутренние напряжения получаемых осадков. Благодаря хорошим физико-химическим свойствам широкую популярность получили лимоннокислые электролиты золочения.
К недостаткам кислых электролитов золочения можно отнести их относительно низкую рассеивающую способность и более высокие внутренние напряжения получаемых осадков. Благодаря хорошим физико-химическим свойствам широкую популярность получили лимоннокислые электролиты золочения.
Состав электролита блестящего золочения:
Дицианаурат калия (K Au(CN2)2) — 20-22 г/л
Комплексное соединение кобальта с ЭДТА -25-27 г/л
Плотность тока до 4,5 А/дм 2 ; рН = 6,5-7,5; температура 20-32 о С.
Состав электролита блестящего золочения (повышенной твердости):
Дицианаурат калия (KAu(CN2)2) 4 г
Сернокислый никель (NiSO4) — 1 г/л
Плотность тока до 1,5 А/дм 2 ; рН = 3,0-4,5; температура 40-50 о С
Оборудование для золочения использующееся в производственных цехах и лабораториях представляет собой регулируемый источник питания постоянного тока с высокой стабильностью, малым уровнем пульсаций, выдающий выходной ток до 20 А и обеспечивающий возможность малого “шага” регулировки до 0.05 А. Для золочения металлов и нанесения золотых покрытий используются нерастворимые аноды: титановая пластина или сетка с иридиевым или платиновым покрытием.
Для покрытия небольших по размеру деталей в гальванотехнике применяется золочение без тока: так называемый метод иммерсионного золочения. Покрытия, полученные методом иммерсионного золочения мало пористы, а время выдержки в электролите, в зависимости от толщины покрытия, составляет от нескольких секунд до нескольких минут. Ванны для иммерсионного золочения обычно изготавливают из стали или стекла.
Состав электролита иммерсионного золочения:
Золото (в пересчете на металл) — 1,2 г/л
Температура электролита 70 о С. Средняя скорость осаждения 1,5 мкм в час.
Выделение золота из отработанных электролитов золочения наиболее часто проводят контактным методом. Для этого, в отработанный электролит добавляют предварительно освинцованную мелкую цинковую стружку (освинцовывание проводят путем опускания стружки на 1 -2 минуты в раствор, содержащий 100 г/л уксуснокислого свинца). Для осаждения золота раствор выдерживают в течении 10-12 дней при комнатной температуре, добавляя в него каждые 2-3 дня, немного цинковой стружки (для проверки полноты осаждения золота, в отработанный электролит золочения на 5-7 мин добавляют порцию блестящей не освинцованной цинковой стружки; если стружка не темнеет, процесс восстановления закончен). Далее электролит фильтруют, оставшийся осадок с остатками стружки промывают, переносят в фарфоровую или стеклянную чашку и просушивают. После этого, осадок обрабатывают соляной кислотой (плотностью 1,19 г/см 3 ), тщательно промывают и затем обрабатывают, нагретой до 35-40 о С, азотной кислотой (плотностью 1,4 г/см 3 ), в результате чего, осадок приобретает цвет металлического золота. Для ускорения осаждения золота, электролит дополнительно разрушают путем добавления в отработанный раствор избытка серной кислоты. Восстановление золота в подкисленном растворе также проводят цинковой стружкой.
Бесцианидные электролиты золочения
Смирнов К.Н., Харламов В.И., доктор химических наук, профессор
Российский химико-технологический университет им. Д.И. Менделеева
ООО «Клио-Техника»
В современной гальванотехнике одной из актуальных задач является замена высокотоксичных цианидных электролитов. Это обусловлено необходимостью улучшения условий труда персонала, повышения безопасности очистки сточных вод и утилизации отработанных растворов.
Разработке новых, в том числе бесцианидных, электролитов золочения уделяется большое внимание. Только в США к настоящему времени разработано более 300 различных электролитов золочения, что значительно превышает количество электролитов для осаждения других металлов. Постоянная модификация растворов во многом вызвана меняющимся спросом на различные цвета и оттенки ювелирных изделий.
Технологии золочения имеют свою специфику, отличающую их от других гальванических процессов. Высокая стоимость электролитов диктует необходимость разработки электролитов с минимальным количеством золота в технологическом процессе. С другой стороны, экономические факторы ограничивают возможности опытных работ в промышленности и заставляют придерживаться хорошо отработанных технологий.
Для обработки ювелирных и декоративно-прикладных изделий в основном применяются различные цитратные электролиты золочения, характеристики которых приведены в таблице (электролит 1). Эти электролиты можно условно назвать бесцианидными, поскольку при их приготовлении не используется цианид калия, а золото вводится в состав растворов в виде цианидных соединений.
Слабокислые цитратные электролиты (электролит 1) не содержат свободного цианид-иона. Золото находится в виде комплекса Au(CN)2 — , который устойчив при рН выше 3. Безусловно, опасность этих электролитов значительно меньше, чем щелочных цианидных. Однако в процессе эксплуатации с нерастворимыми анодами возможно накопление в электролите небольших количеств свободных CN — . Цитратные электролиты имеют ряд технологических недостатков, таких как низкая рассеивающая способность, накопление в электролите продуктов анодного окисления органической кислоты.
Известны составы электролитов, приготовленных на основе хлорного золота и гексацианоферрата(II) калия (железистосинеродистого калия) (электролит 2). Данные электролиты также можно отнести к условно бесцианидным, так как ионы золота находятся в цианидном комплексе, а при эксплуатации в растворе может накапливаться цианистый калий.
Имеются сведения о разработке электролитов на основе меркаптоалкилсульфоновых кислот, растворов на основе HAuCl4, 1,2 — этилендиаминзолотохлорида, комплексов ионов золота с аминокислотами. Однако сведений о промышленном применении данных электролитов нет.
В начале 1960-х гг. были разработаны составы электролитов, в которых золото присутствует в виде дисульфитаурата натрия — Na3(Au(SO3)2) (электролит 3). Для повышения электропроводности и улучшения буферных свойств растворов рекомендуется применять соли фосфорной, уксусной или винной кислот. Такие электролиты позволяют получать покрытия сплавами на основе золота от 12 до 24 карат.
Золотые покрытия, осаждающиеся из сульфитных электролитов, имеют крупнокристаллическую структуру. В качестве добавок, обеспечивающих осаждение мелкокристаллических и даже блестящих покрытий, в электролиты вводят небольшие (0,1-50 мг/л) количества солей мышьяка, таллия, сурьмы, селена или свинца. Однако применение таких добавок в отсутствие высокоточного аналитического контроля электролитов затруднено. Следует отметить, что накопление ионов этих металлов до 1г/л приводит к потемнению покрытий и формированию рыхлых осадков.
Сульфитные электролиты позволяют наносить золотые покрытия с высокой микротвердостью (1300-1400 МПа), что очень важно для изделий, подвергающихся механическим нагрузкам. При необходимости микротвердость покрытий можно снизить до 900 Мпа, уменьшив рН электролита до 6-7.
К достоинствам сульфитных электролитов следует отнести высокую микро- и макрорассеивающую способности и возможность получать блестящие покрытия сплавами с высокой пластичностью.
Одним из существенных недостатков сульфитных электролитов золочения, затрудняющих их практическое применение, является их нестабильность. В процессе хранения электролита происходит постепенное окисление сульфита до сульфата кислородом воздуха. Для предотвращения быстрого окисления сульфита в процессе электролиза необходимо регулировать площадь нерастворимых анодов, чтобы соотношение анодной и катодной поверхности составляло не менее 1:1.
Кроме того, сульфит-ионы восстанавливаются на катоде до S2O4 2- , которые в свою очередь восстанавливают Au(I) до металла. Для удаления мелкодисперсных частиц металлического золота из объема электролита необходимо периодически применять фильтрацию.
Одной из проблем при эксплуатации бесцианидных электролитов является обеспечение надежного сцепления золотых покрытий с подслоем никеля, который используется для предотвращения взаимной диффузии металлов основы и покрытия, а также для обеспечения декоративных характеристик. Для сульфитных электролитов сцепление покрытия улучшается при повышении температуры электролитов до 50-70 °С. Однако и в этом случае рекомендуется наносить на изделия подслой золота из разбавленного цианидного электролита или наносить слой никель-страйк, что неизбежно ухудшает блеск покрытий.
В настоящее время сульфитные электролиты золочения, предлагаемые различными фирмами, составляются на основе жидких золотосодержащих концентратов или сухих препаратов. При изготовлении золотосодержащих компонентов в качестве стабилизаторов используются вещества, образующие более прочные полилигандные сульфитные комплексы золота, например, алифатические амины, или вещества, способные подавлять реакцию диспропорцианирования свободных ионов Au(I) за счет образования прочных комплексов — купферон, железистосинеродистый калий. Однако, приготовление сульфитных электролитов без специального оборудования весьма трудоемко и связано с большими потерями драгоценного металла (до 40%). В специализированных фирмах потери металла при получении золотосодержащего препарата в твердом состоянии не превышают 2-3%.
Несмотря на то, что сульфитные электролиты в целом отвечают современным требования экологической безопасности, они не нашли широкого применения в ювелирной промышленности из-за малой эффективности и трудностей в эксплуатации.
Для бесцианидных и условно бесцианидных электролитов золочения в качестве нерастворимых анодов рекомендуется использовать платинированный титан, или титан с нанесенным слоем оксида рутения (ОРТА). При использовании нержавеющей стали следует учитывать, что в процессе эксплуатации происходит растворение железа и никеля , постепенное их накопление в растворе и ухудшение качества золотых покрытий. Для снижения скорости растворения стали рекомендуется применять низкие анодные плотности тока.
В слабокислых электролитах золочения на нерастворимых анодах происходит окисление лимонной кислоты до ацетодикарбоновой кислоты, которая затем декарбоксилируется с образованием ацетона. При неправильно выбранном режиме электролиза в объеме раствора могут образовываться белые хлопьевидные продукты окисления лимонной кислоты, которые захватываются катодным осадком золота, ухудшая качество покрытий. Большинство исследователей рекомендует в этом случае оптимальное соотношение катодной и анодной поверхности от 1:1 до 1:1,5.
Таким образом, разработка новых и совершенствование известных бесцианидных электролитов золочения остается актуальной задачей, решение которой обеспечит их широкое применение в ювелирной промышленности.

